우리 몸의 DNA는 선조들이 하던 대로 과잉 에너지를 적극 저장하라고 명령하고, 결국 우리가 미워하고 두려워하는 살이 불어날 위험에 처하게 만든다. 체내에 저장된 에너지가 과도하게 많아져 비만이 되면 고혈압, 당뇨, 대사증후군 등이 생기고, 생존을 위해 저장했던 에너지는 역설적으로 우리의 생존을 위협할 수 있다.
어떻게 해야 체내 에너지 공급이 균형을 이루도록 유지할 수 있을까? 먹고자 하는 욕구, 즉 식욕을 이해한다면 과도한 살 문제를 해결해줄 단서를 찾을지도 모르겠다. 대부분의 욕구가 뇌의 활동으로부터 발생하고 조절되듯이, 식욕도 뇌의 작용을 바탕으로 일어난다. 그렇다면 인간의 뇌는 몸에 에너지가 부족한지 과잉인지 어떻게 알아채며, 어떤 근거로 음식을 더 먹거나 그만 먹으라고 명령을 내리는 걸까.
살아있는 생명체가 생명 현상을 유지하는 데 가장 필수적인 것은 다름 아닌 에너지원의 공급이다. 문제는 먹을 것이 항상 풍족하게 공급되는 것은 아니라는 점이다. 따라서 그간 생명체의 몸은 에너지를 최소한으로 사용하고, 남은 영양분을 저장해 추후 먹을 것이 없을 때를 대비할 수 있도록 진화해왔고, 이를 통해 성공적으로 생존할 수 있었다.
우리의 선조도 바로 그런 개체였다. 그리고 우리는 그들의 DNA를 그대로 물려 받아 살고 있다. 그런데 긴 시간이 흐르면서 상황이 바뀌었다. 이른바 선진국으로 꼽히는 국가에 거주하는 현대인은 넘치는 식욕을 채우고도 남을 만큼 먹을 것이 풍부한 시대에 살고 있다. 우리 뇌는 이런 변화에 어떻게 대처하고 있을까.

식욕 ‘호르몬 형제’ , 렙틴과 그렐린
뇌의 작용은 자세히 모르더라도 식욕이 언급될 때마다 자주 등장해 대중에게 친숙한 ‘호르몬 형제’는 들어봤을 것이다. 바로 식욕 억제 호르몬 렙틴(leptin)과 그 반대 작용을 담당하는 그렐린(ghrelin)이다. 렙틴은 지방세포에서, 그렐린은 위장에서 나온다.
먼저 렙틴을 살펴보자. 이 단어는 ‘날씬하다’는 뜻의 그리스어 ‘렙토스’에서 유래됐는데, 이름만으로도 그 기능을 추측할 수 있다. 날씬하게 만드는 물질, 즉 식욕을 억제해 적게 먹도록 하는 호르몬이다.
1973년 더글라스 콜먼 미국 잭슨실험실(The Jackson Laboratory) 교수는 고도비만 또는 당뇨에 걸린 생쥐에 있는 obese(ob)와 diabetes(db) 유전자 돌연변이를 연구하면서 ob 유전자가 만들어 낸 혈중 OB 단백질이 db 유전자가 만들어 낸 DB 단백질에 작용해 식욕을 감소시킨다는 사실을 발견했다. doi: 10.1007/BF01221857 식욕에 영향을 주는 호르몬의 존재 가능성을 처음으로 언급한 것이다.
이후 1995년 제프리 프리드먼 미국 록펠러대 교수는 ob 유전자가 지방세포에서 만드는 단백질이 체중을 줄이는 기능을 한다는 사실을 규명하고 이를 ‘렙틴’으로 명명했다. doi: 10.1126/science.7624777
렙틴이 부족한 생쥐에 렙틴을 투여했더니 음식 섭취량이 줄어 정상 체중으로 돌아온 것이다. 렙틴 유전자에 이상이 생겨 고도비만이 된 환자에게 렙틴을 투여하자 체중 감량 효과를 확인한 사례도 학계에 보고됐다. 콜먼 교수와 프리드먼 교수는 렙틴을 발견한 공로로 2010년 미국의 노벨상으로 불리는 래스커상을 수상했다.
하지만 수수께끼 같은 문제가 남아 있었다. 대부분의 비만 환자에게 렙틴을 투여해도 그 효과가 미미하다는 점이었다. 또 비만한 사람에서는 대부분 렙틴이 부족한 것이 아니라 오히려 많다는 사실이 확인됐다.
현재 학계에서는 이를 ‘렙틴 저항성’이라고 부른다. 비만일수록 렙틴이 결합하는 수용체에 변화가 생기거나 세포 내 렙틴의 신호전달체계에 문제가 발생해 그 기능을 잃어버리게 된 것이다. 이는 체내에 염증 신호가 증가하거나, 지방산이 증가하거나, 렙틴이 지나치게 높게 유지되는 것이 원인이다.
렙틴 저항성을 회복하기 위해서는 가공식품을 적게 먹고, 식이섬유를 많이 먹으며, 운동을 늘리고, 잠을 충분히 자는 것이 중요하다.
특히 중성지방은 렙틴이 뇌 속으로 전달돼 식욕이 줄어드는 것을 방해한다. 탄수화물 섭취를 줄이면 중성지방을 줄일 수 있고, 단백질 섭취를 늘리는 것은 렙틴의 활성을 높인다. 일반적으로 얘기하는 건강한 생활 습관이 모두 렙틴 저항성을 극복하는 데 도움이 된다는 사실이 우연의 일치는 아닌 듯하다.
과도한 식욕도 문제지만 반대로 식욕이 너무 없는 것도 문제가 될 수 있다. 비정상적으로 잘 먹지 않으려고 하는 신경성 식욕부진증(anorexia nervosa)을 자칫 가볍게 여길 수 있는데, 실제로 이는 사망률이 5.9%에 이르는 무서운 질병이다.
신경성 식욕부진증이 발생하는 이유는 사회심리적 원인과 더불어 유전적, 신경생물학적 원인이 복합적으로 작용한다고 알려져 있다. 식욕을 촉진하는 그렐린이라는 호르몬이 위장에서 합성돼 뇌에 전달되면 공복감과 함께 식욕을 느끼게 된다. 그런데 신경성 식욕부진증 환자에서는 그렐린 수치가 비정상적으로 높은 상태인 경우가 많다. 그래서 학계에서는 ‘그렐린 저항성 가설’이 제기되고 있다.
이와 함께 그렐린의 상승과 연동된 보상회로가 작동되는 것도 이 질환의 원인으로 지목되고 있다. 배고픈 느낌을 지속적으로 갈망하고 공복감 자체에 중독되는 현상이 나타나는 것이다.
식욕 조절의 주연과 조연 신경세포
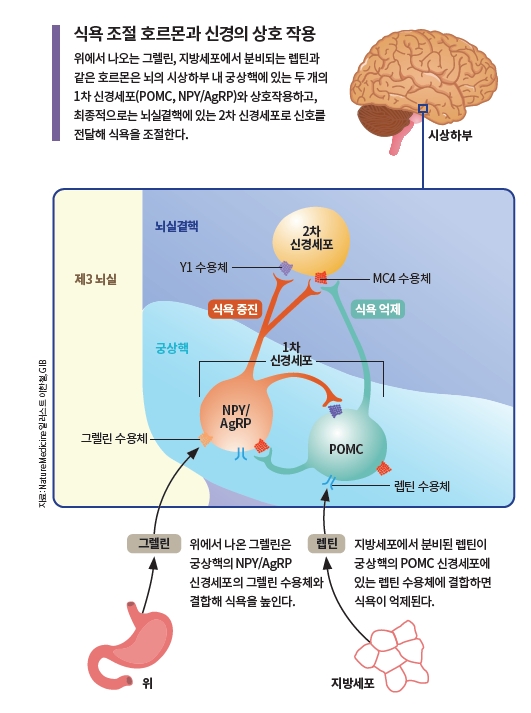
지방세포에서 나오는 렙틴과 위장에서 나오는 그렐린이 향하는 곳은 어디일까. 이들은 모두 뇌의 시상하부의 궁상핵(arcuate nucleus)에 작용한다. 궁상핵이 식욕과 식이행동을 조절하는 중요한 컨트롤타워인 셈이다.
특히 궁상핵에 존재하는 POMC(proopiomelanocortin) 신경세포와 NPY/AgRP(neuropeptide Y/agouti-related peptide) 신경세포는 각각 식욕 조절의 ‘주연’과 ‘조연’을 번갈아 담당할 만큼 중요한 역할을 한다.
POMC 신경세포는 식욕을 억제하고, NPY/AgRP 신경세포는 식욕을 증가시키는 것이 기본 역할이다. 그래서 렙틴은 POMC 신경세포를 활성화시키고, 그렐린은 NPY/AgRP 신경세포를 활성화시킨다.
이런 작용들을 통해 궁상핵의 신경세포들이 최종적으로 뇌실곁핵에 있는 2차 신경세포 위 메라노코르틴(MC)4 수용체(식욕 억제)나 Y1 수용체(식욕 증진)로 신호를 보내면 식욕이 조절된다.
식욕조절에서 최근 주목받고 있는 호르몬이 하나 더 있다. 장에서 합성되는 호르몬인 ‘글루카곤 유사 펩타이드(GLP)-1’다. GLP-1은 혈당 조절에 중요한 호르몬 중 하나다. 혈당을 낮추는 호르몬인 인슐린의 분비를 촉진하고, 혈당을 높이는 호르몬인 글루카곤의 분비를 억제해 결과적으로 혈당을 낮게 유지하는 데 도움을 준다.
GLP-1이 궁상핵에서 식욕을 조절하는 데 중요한 역할을 한다는 사실은 지난해 밝혀졌다. 식욕 억제에 관여하는 POMC 신경세포는 GLP-1 수용체를 가지고 있는데, GLP-1이 이 수용체에 결합하면 세포를 활성화시켜 식욕억제 효과가 일어난다.
따라서 렙틴 저항성이 있는 비만 환자에서도 약물로 GLP-1 수용체를 활성화시켜 POMC 신경세포를 활성화시킬 수 있다. 또 GLP-1은 NPY/AgRP 신경세포를 억제하는 역할을 하는 신경세포를 활성화시켜, 결과적으로 NPY/AgRP 신경세포를 억제하는 기능도 간접적으로 수행한다. doi: 10.1016/j.molmet.2019.07.008
GLP-1은 이런 식으로 궁상핵의 주연과 조연에 모두 작용해 강력한 식욕 억제 효과를 유도한다. 현재 이런 원리를 이용한 약물이 시판되고 있으며, 효과적인 식욕 억제 기능 덕분에 2형 당뇨병과 비만 치료제로도 사용되고 있다.
이밖에도 2017년에는 뼈를 합성하는 세포인 조골모세포가 분비하는 리포칼린(lipocalin)-2라는 호르몬이 뇌실곁핵에 있는 MC4 수용체에 작용해 식욕을 억제한다는 사실이 확인돼 국제학술지 ‘네이처’에 실렸다.
같은 해 국제학술지 ‘사이언스’에는 지방세포에서 분비되는 유리딘(Uridine·RNA의 구성성분으로 대사에 관여)이 금식을 할 때 증가하는데, 그 결과 체온을 낮추고 산소 사용량을 줄여 에너지 소비를 최소화하면서 렙틴의 분비를 억제해 식욕이 증가하도록 조절한다는 사실도 확인됐다. doi: 10.1126/science.aaf5375
위장과 지방세포처럼 인체의 말초 부위에서 합성된 물질들이 뇌에 도달해 뇌의 기능을 조절한다는 사실은 몸과 뇌, 다시 말해 몸과 마음이 연결돼있음을 시사한다고 볼 수 있다.
현재 뇌과학 연구는 비만이나 식욕에 대한 이해를 급속히 넓혀가고 있다. 아직은 밝혀지지 않은 미지의 부분도 많지만 언젠가 퍼즐이 좀 더 맞춰져 누구나 건강하게 먹고 건강하게 지낼 수 있는 뇌과학적 해결책을 찾게 되길 기대해본다.
*용어정리
뇌실곁핵 (paraventricular nucleus): 시상하부의 앞쪽 셋째 뇌실벽에 있는 신경세포 집단.
2형 당뇨병 (Type 2 diabetes) : 췌장에서 인슐린이 분비되지 않는 1형 당뇨병과 달리, 2형 당뇨병은 인슐린이 분비되기는 하지만 혈당량을 조절하는 기능을 제대로 수행하지 못하는 질환이다.
※필자소개
김태. 경희대 의대에서 박사학위 및 정신건강의학과 전문의를 취득하고, 미국 하버드대 의대 정신건강의학과에서 박사후연구원을 지냈다. 현재 광주과학기술원(GIST) 의생명공학과 교수로 재직 중이다. 최근에는 수면장애, 알츠하이머병, 자폐증에 대한 뇌과학 연구를 수행하고 있다. tae-kim@gist.ac.kr