“이제 태양광에너지는 더 이상 대체에너지가 아닙니다.” 대전 한국화학연구원(이하 화학연) 에너지소재연구센터 문상진 박사는 화석연료를 기준으로 한 대체에너지란 용어가 머지않아 사라질 거라고 전망했다. 제한된 매장량에 중동과 북아프리카 정세 불안이 겹쳐 기름값은 해가 다르게 오르는 반면 태양광을 이용하는 기술은 눈부시게 발전하고 있기 때문이다.
지구촌 사람들이 1년에 사용하는 에너지의 양은 어마어마해 보이지만 지구에 도달하는 태양에너지 양의 0.01%에 불과하다. 광합성을 하는 미생물과 식물이 태양에너지의 극히 일부를 이용할 뿐 대부분은 대기나 지표에서 반사돼 다시 저 멀리 우주로 향한다. 따라서 지구에 도달하는 태양 에너지를 ‘경제성 있게’ 활용하는 방법을 찾으면 인류는 에너지 위기에서 벗어날 수 있다.

석유 수준에 다가가는 경제성
“지난해 세계 최초로 6세대 다결정 실리콘 잉곳을 양산하는 시스템을 개발하는 데 성공했습니다. 5월 상용화될 예정인데 실리콘 웨이퍼의 단가가 더 떨어지겠죠.”
실리콘 잉곳(ingot)이란 실리콘 결정으로 이뤄진 덩어리로 가로세로 길이가 같고 납작한 6면체다. 6세대란 이 잉곳을 가로세로 6등분한다는 뜻으로 전부 36개의 ‘벽돌’이 나온다. 이 벽돌을 두께 200μm(마이크로미터, 100만분의 1m)로 썰어낸 게 실리콘 웨이퍼다.
“실리콘 웨이퍼 타입 태양전지의 작동원리는 광반도체와 똑같다고 보면 됩니다. 빛을 받으면 전자가 높은 에너지 상태가 돼 한쪽 전극으로 이동하면서 전압이 생깁니다.”
현재 실리콘 웨이퍼 타입은 전체 태양전지의 80% 이상을 차지하고 있다. 에너지 효율이 15% 정도로 높고 오랫동안 쓸 수 있기 때문이다. 2~3년 전만해도 1와트의 전력을 생산하는 비용이 3.5달러 수준이었지만 현재는 1.8달러까지 떨어졌다. 물론 1달러 수준인 석유보다는 여전히 높지만 제조비용이 더 떨어지고 유가가 더 오르면 역전될 수도 있다.
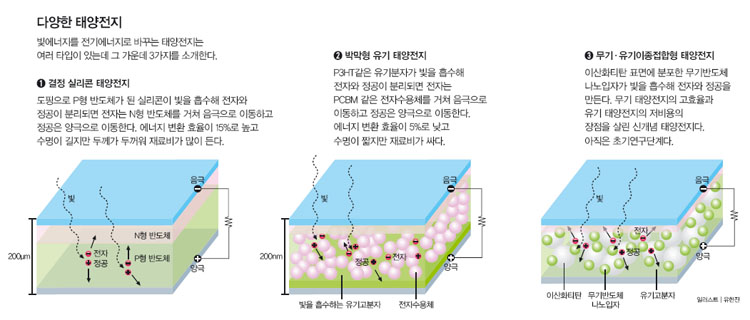
문 박사팀은 실리콘 같은 무기 태양전지뿐 아니라 유기 태양전지도 연구하고 있다. 유기 태양전지는 에너지 전환 효율이 낮고 내구성도 떨어지지만 만들기가 쉽고 비용도 훨씬 덜 든다는 장점이 있다. 유기 태양전지는 말 그대로 유기반도체 분자가 빛을 흡수한다. 이렇게 유기분자에서 에너지가 높아진 전자는 풀러렌처럼 전자를 잘 끌어당기는 분자로 이동하면서 전압을 만든다.
문 박사는 “유기 태양전지는 휘어지는 필름형태로 만들 수 있기 때문에 텐트나 가방 등 일상용품에 붙여 소규모 전력을 생산할 수 있다”고 설명했다.
화학연 소자나노재료연구센터의 석상일 박사는 새로운 개념의 태양전지를 개발하고 있다. ‘나노구조 무기·유기이종접합형 태양전지’가 그것으로 무기 태양전지의 고효율과 유기 태양전지의 저비용이라는 장점만을 살린다는 계획이다. 연구자들은 빛을 흡수해 전자와 정공을 만드는 무기 반도체인 황화안티몬(Sb2S3)을 나노입자 형태로 만들어 치약 같은 상태인 이산화티탄 표면에 발랐다. 여기에 정공을 전달하는 P3HT라는 유기고분자층을 만들어 붙인 뒤 햇빛을 쪼여주자 황화안티몬에서 생성된 전자는 이산화티탄쪽으로 흐르고, 동시에 정공은 P3HT쪽으로 흘러 태양전지가 작동한다.
석 박사는 “나노입자의 순도가 높지 않아도 작동하는 데 별영향이 없다”며 “아직은 시스템이 최적화되지 않아 효율이 낮은 편이지만 가능성이 확인된 만큼 미래는 밝다”고 말했다.

➊ 한국화학연구원이 세계 최초로 양산화에 성공한 6세대 실리콘잉곳. 36개의 벽돌로 자른 상태다.
➋ 가로세로 15.6cm인 벽돌을 두께 0.2mm로 썰어내 웨이퍼를 만든다. 이 웨이퍼를 가공해 태양전지를 만든다.
인공 광합성 꿈꾼다
“태양에너지를 이용해 유용한 화합물을 만들면서 온실기체인 이산화탄소도 줄일 수 있는 방법이 바로 광합성이죠.”
강영수 서강대 화학과 교수는 요즘 인공광합성 연구에 ‘올인’했다. 강 교수는 지난해 문을 연 ‘인공광합성연구센터’의 부소장(같은 과 윤경병 교수가 소장)을 맡고 있다. 인공광합성이란 자연의 광합성과 비슷하게 햇빛을 이용해 물, 이산화탄소로부터 유기화합물을 만드는 과정이다. 둘의 가장 큰 차이점은 식물은 포도당을 만드는 반면 인공 광합성은 메탄올이나 일산화탄소처럼 간단한 화합물을 생산한다는 데 있다.
“인공광합성은 크게 3단계로 이뤄지는데 매 단계에서 충분한 효율성이 확보돼야 상용화될 수 있습니다.”
인공광합성은 빛에너지로 물분자를 쪼개 전자와 양성자(수소이온)를 얻는 1단계, 전자와 양성자를 옮기는 운반체를 만드는 2단계, 운반된 전자와 양성자에 이산화탄소를 반응시켜 화합물을 얻는 3단계로 이뤄진다. 그런데 자연이 수십 억 년에 걸쳐 최적화한 광합성 방법을 모방하기만 하면 문제는 쉽게 풀리는 게 아닐까.
“물론 그런 연구를 하기도 합니다. 하지만 식물의 광합성은 세포 안에서 일어나는 아주 복잡한 반응이기 때문에 이를 재현하기 어렵죠.”
1단계 연구에 참여하고 있는 경북대 에너지공학부 박현웅 교수의 설명이다. 식물은 엽록소라는 분자의 전자가 빛에너지를 흡수해 에너지가 높아진 뒤 주변 분자로 이동한다. 엽록소의 전자가 부족해져(이를 ‘정공’이라고 부른다) 물분자를 분해해 전자를 빼앗는다. 이 과정에서 산소와 양성자가 함께 만들어진다. 엽록체에서 이런 반응이 일어나는 부분이 ‘광반응계Ⅱ’다.
박 교수팀은 철산화물처럼 빛을 흡수하는 산화물반도체에 물분자를 분해하는 반응이 쉽게 일어나게 하는 촉매를 붙인 시스템을 만들어 광반응계Ⅱ의 역할을 재현하고 있다. 현재 산화물반도체와 촉매의 구조를 바꿔가며 최적의 효율을 보이는 조성을 찾고 있다.
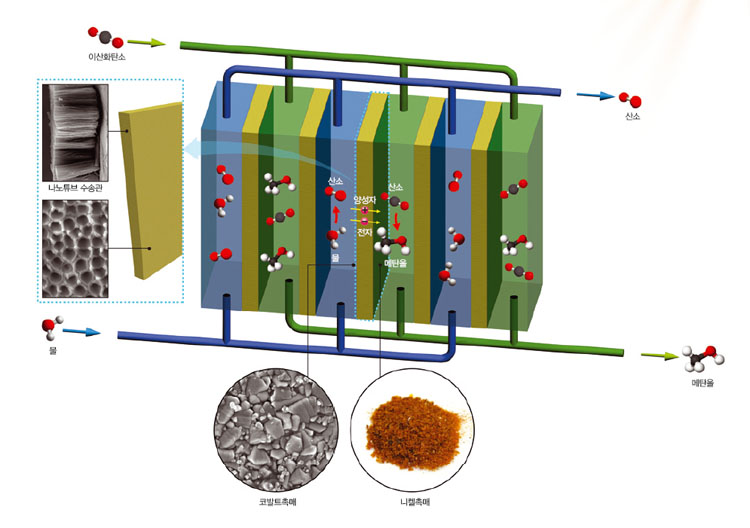
강영수 교수팀은 1단계에서 만들어진 양성자와 전자를 3단계 반응이 일어나는 장소로 옮기는 시스템을 연구하고 있다. 식물에서는 생체분자인 NADP+가 NADPH로 환원돼 이동하면서 이 역할을 하지만 인공광합성에서는 나노튜브수송관을 통해 전자와 양성자를 따로 이동시키는 방법을 연구하고 있다.

강 교수는 “인공광합성 효율을 끌어올리려면 집적된 형태의 시스템을 만들어야 하기 때문에 나노기술이 필요하다”고 설명했다.
한편 서강대 화학과 신운섭 교수팀은 이렇게 얻은 전자와 양성자에 이산화탄소를 더해 유기화합물을 만드는 3단계 연구를 진행하고 있다. 포름산과 일산화탄소를 만드는 데 성공했고 현재 메탄올을 만드는 반응을 실험하고 있다. 여기서도 관건은 역시 촉매다. 촉매의 종류와 구조에 따라 만들어지는 화합물의 종류와 효율이 결정되기 때문이다. 연구팀은 니켈화합물과 구리화합물에 기반한 촉매를 개발하고 있다.
신 교수는 “태양에너지에서 유기화합물을 만드는 데까지 효율이 1%만 되도 상용화가 가능하다”며 “현재는 0.1%도 안 되는 수준이지만 이제 막 시작한 분야이므로 미래는 밝다”고 말했다.
제올라이트 촉매로 나프타 분해
“어이쿠!”
“촉매가 바닥에 좀 떨어졌네요. 입자 지름이 머리카락 두께 정도 밖에 안 되지만 공 형태라 미끄럽습니다. 조심하세요.”
대전 한국화학연구원 그린(녹색)화학연구단 박용기 박사의 안내로 새로운 나프타분해공정 파일럿플랜트를 둘러보던 기자는 하마터면 미끄러져 엉덩방아를 찧을 뻔했다. 바닥을 보니 밀가루처럼 하얀 가루가 흩어져 있다. 파일럿 플랜트란 실험실에서 성공한 반응을 대형 플랜트로 상용화하기 전에 중간 단계로 규모를 키운 설비다. 파일럿플랜트를 거치지 않고 곧바로 상용플랜트를 만들었다가 반응이 재현되지 않으면 엄청난 손해를 보기 때문이다.
나프타란 원유에서 정제한, 탄소 5~7개로 이뤄진 탄화수소분자 혼합물로 이를 분해해 플라스틱 원료인 에틸렌(탄소2개)과 프로필렌(탄소 3개)을 얻는다. 그렇다면 나프타를 어떻게 분해할까. 생각보다 단순하다. 1000℃에 가까운 뜨거운 통 속에 나프타를 넣어주면 ‘열 받은’ 분자가 쪼개진다.
이를 ‘열분해’ 공정이라고 부른다. 이런 식으로 만들다보니 에틸렌이나 프로필렌 100t을 얻는데 석유 40t이 소모된다. 따라서 발생하는 이산화탄소의 양도 엄청나다.

“저희는 제올라이트 촉매를 이용해 좀 더 낮은 온도인 650℃에서 나프타분해가 일어나는 공정을 개발했습니다. 그 결과 이산화탄소 발생량을 20% 줄일 수 있었죠.”
제올라이트는 규소나 알루미늄 산화물이 다공성 구조를 이루고 있는 물질로 표면적이 매우 넓다(제올라이트 10g의 표면적은 축구장 넓이다). 따라서 기화된 나프타 분자가 제올라이트 촉매를 통과할 때 표면에서 분해반응이 일어난다.
박 박사는 “실험실에서 이런 반응이 일어나게 하는 건 그렇게 어렵지 않다”며 “문제는 이런 공정의 규모를 키웠을 때 나타나는 예기치 못한 상황을 해결하는 것”이라고 설명했다. 실제로 초기에는 제올라이트 촉매가 반응을 반복하면서 파괴되거나 활성이 떨어져 반응 효율이 낮았다. 박 박사팀은 제올라이트의 성분과 구조를 바꿔가며 최적의 조합을 찾았다. 그 결과 650℃에서 장시간 버틸 수 있을 정도로 안정하면서도 활성을 유지하는 촉매를 개발했다.
지난해 SK이노베이션은 박 박사팀과 개발한 나프타 촉매분해 공정을 채택한, 연간 생산량 4만t 규모의 설비(데모플랜트)를 만들었고 6개월에 걸쳐 테스트해 긍정적인 결과를 얻었다. SK이노베이션은 현재 연간 생산량 100만t 규모의 상용 플랜트를 짓는 방안을 검토하고 있다. 같은 연구단의 전기원 박사팀은 메탄과 이산화탄소로 메탄올을 만드는 야심찬 프로젝트를 진행하고 있다. 메탄올은 휘발유첨가제나 바이오디젤을 만들 때 들어가는 원료로 산업계의 수요가 꾸준히 늘고 있다. 현재는 천연가스(메탄)와 물을 섞어 반응시켜 메탄올을 만들고 있다.
전 박사팀이 설계한 반응은 메탄과 물에 이산화탄소를 추가로 섞어 메탄올을 만드는 방법이다. 이 방법을 쓰면 메탄 3분자와 이산화탄소 1분자에서 메탄올 4분자를 얻을 수 있다. 기존 방법은 메탄 4분자에서 메탄올 4분자를 얻는다. 이산화탄소가 원료로 들어가니 연료가 연소될 때 나오는 이산화탄소가 줄어드는 셈이다.
이 반응은 두 단계로 이뤄지는데 1단계에서는 메탄, 물, 이산화탄소를 반응시켜 일산화탄소와 수소를 얻고 2단계에서는 일산화탄소와 수소를 반응시켜 메탄올을 얻는다. 전 박사는 “각 단계의 반응에서 촉매가 중요한데 1단계에서는 수십 나노미터 크기로 만든 니켈과 마그네슘 촉매를, 2단계에서는 구리와 아연 촉매를 쓰고 있다”며 “현재 우리나라에서 사용하는 메탄올을 이 공정으로 만든다면 연간 20만t의 이산화탄소 감소 효과가 있다”고 설명했다.