
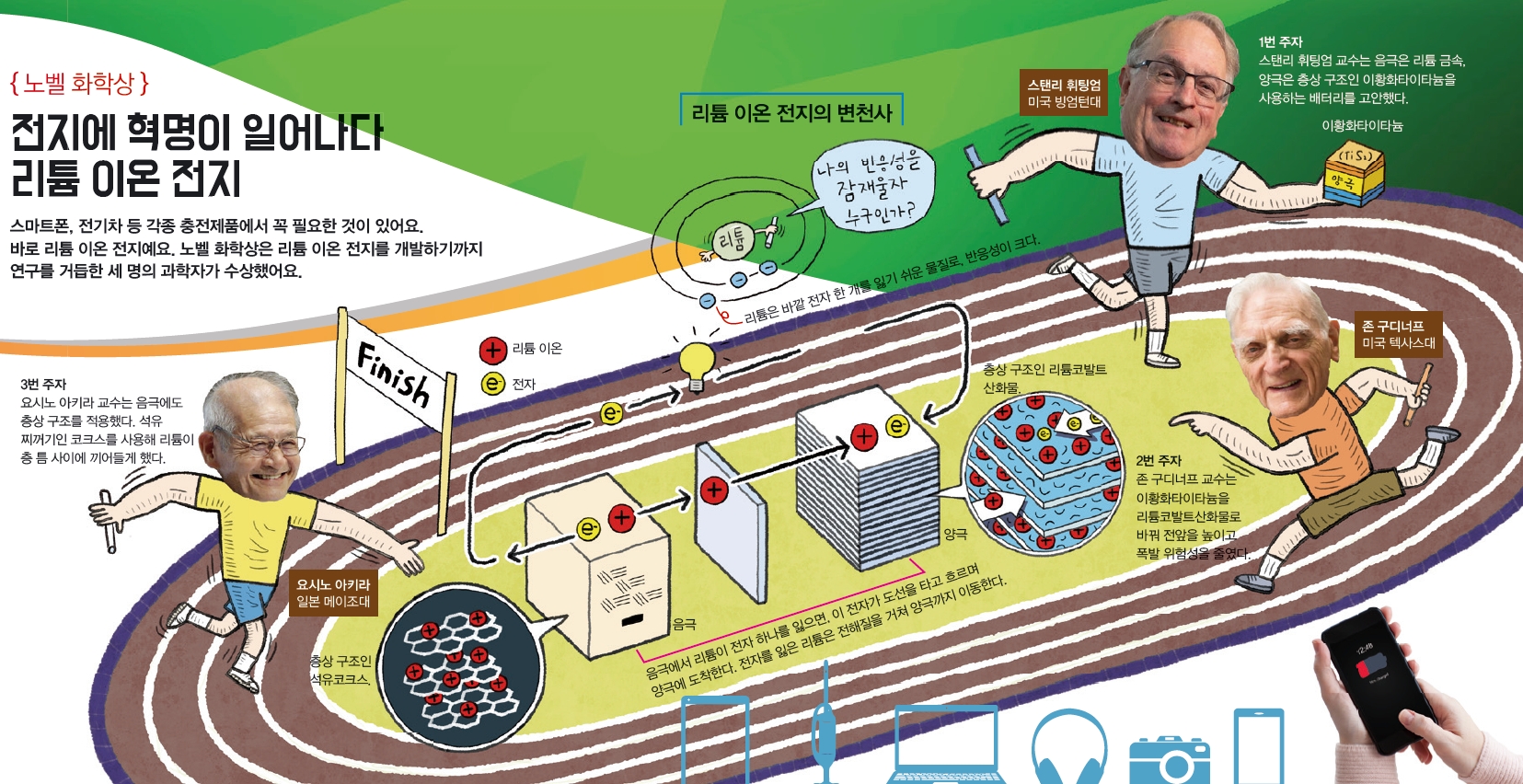
스마트폰, 전기차 등 각종 충전제품에서 꼭 필요한 것이 있어요. 바로 리튬 이온 전지예요. 노벨 화학상은 리튬 이온 전지를 개발하기까지 연구를 거듭한 세 명의 과학자가 수상했어요.
1970년대 중동 지역에 전쟁이 일어나 석유 값이 폭등하는 사건이 두 차례 벌어졌어요. 이에 휘발유 대신 전기로 움직이는 전기자동차가 주목받았지요. 그런데 전기자동차를 상용화하기 위해선 우선 성능이 좋은 전지가 필요했어요. 이에 1972년 당시 미국의 석유 기업에 다니고 있던 스탠리 휘팅엄 교수는 리튬 금속을 이용한 전지를 고안해냈지요.
반응성이 다른 두 금속을 전해질에 담그고 도선으로 연결하면 전류가 흘러요. 반응성이 큰 금속이 전자를 잃으면, 이 전자가 도선을 따라 반응성이 낮은 금속으로 이동하기 때문이죠. 리튬(Li)은 전자 하나를 잃기 쉽고 가벼워서 배터리의 후보 물질로 꼽혀왔지요. 하지만 리튬의 반응성은 장점인 동시에 단점이었어요. 리튬이 다른 물질과 반응하면 성능이 떨어지고, 심지어는 폭발까지 일어날 수 있거든요.
휘팅엄 교수는 층상 구조인 이황화타이타늄(TiS2)을 사용해 이 문제를 해결했어요. 음극에서 전자를 잃은 리튬 이온이 양극에 도착하면 이황화타이타늄 층 사이로 끼어 들어가 리튬 이온이 외부와 반응하지 못해 위험성이 낮아져요. 하지만 휘팅엄 교수가 고안한 전지는 전압이 2V에 불과했어요. 황(S)이 외부의 산소와 반응한다는 단점도 있었지요. 1980년 존 구디너프 교수는 이황화타이타늄 대신 리튬코발트산화물(LiCoO2)을 사용해 전압을 높였어요. 리튬코발트산화물도 이황화타이타늄처럼 층상 구조인데, 두 배의 전압을 얻을 수 있어요.
마지막으로 1985년 전지를 개발하는 회사에 다니고 있던 요시노 아키라 교수는 음극을 개선했어요. 음극에도 양극과 마찬가지로 층상 구조를 적용했어요. 석유코크스로 리튬 이온을 층 사이에 가뒀지요. 그 결과 리튬 이온은 두 전극 모두에서 층 사이에 갇혀 외부와는 반응하지 않게 되었답니다. 아키라 교수가 완성한 전지가 바로 현재 쓰고 있는 ‘리튬 이온 전지’의 구조예요.
 ▲PDF를 클릭하면 상세내용을 확인할 수 있습니다
▲PDF를 클릭하면 상세내용을 확인할 수 있습니다
세 과학자들이 성능 좋은 전지를 개발한 덕분에 선 없는 전자제품의 시대가 열렸어요. 이런 공로를 인정받아 세 과학자는 올해 노벨 화학상을 수상했지요. 현재 과학자들은 소재를 조금씩 바꿔 배터리의 성능을 높이는 연구를 계속하고 있답니다.











