AIDS 원인바이러스의 외피는 너무나 변이가 심해서 바이러스마다 그 모양이 다를 뿐더러 같은 바이러스라 할지라도 시간이 경과함에 따라 제멋대로 변한다. 이같은「미꾸라지」바이러스를 잡기 위해서는…
AIDS(Acquired Immuno Deficiency Syndrome) 즉 후천성 면역결핍증은 지금부터 약 12년 전인 1981년에 미국의 로스앤젤레스 뉴욕 샌프란시스코 등의 도시에서 처음으로 환자발생이 보고된 이래 전세계에 걸쳐 급속도로 확산되고 있다. 이제는 세계보건기구(WHO)에 공식보고된 숫자만 해도 50만명을 넘어섰다.
여기서 말하는 AIDS환자는 AIDS를 일으킨 원인 바이러스인 인간면역결핍바이러스(Human Immunodeficieny Virus, HIV-1과 HIV-2가 알려져 있다)에 감염되어 생기는 병의 마지막 단계에 있는 사람들로서 실제 바이러스에 감염돼 있는 사람(HIV감염자) 숫자는 이보다 훨씬 많은 1천2백만명 이상일 것으로 추산되고 있다.
우리나라에서도 1985년에 첫 환자가 발견된 이래 작년 10월 말 현재 총 2백35명의 감염자와 10명의 환자가 발생했다.
우리나라에서 밝혀진 감염자의 남녀비율은 6.3 대 1로 남자가 훨씬 많고, 연령은 20, 30대가 78%로 대부분을 차지하고 있다. 우리나라에서 HIV의 감염경로를 보면, 성관계를 통한 것이 역시 압도적으로 많아 전체의 91.7%를 차지하고 있다. 그중 남성동성연애자간의 성관계를 통한 경우가12%, 이성간 성교를 통한 경우가 78%로 후자가 압도적으로 많음을 알 수 있다.
HIV의 표적
1984년 이전까지는 AIDS의 치료는 여기에 수반되는 각종 기회감염이나 종양에 대한 치료에 국한돼 있었다. 그러나 HIV가 원인바이러스임이 밝혀지고, 그 생활사(life cycle)추적과 분자생물학적 연구의 진전에 따라 이 바이러스에 특이적인 항(抗)바이러스요법(antiretrovirus therapy)이 발전하게 되었다. 이때부터 새로운 항바이러스제를 개발하고 적절한 사용법을 발견하려는 전세계적인 노력이 경주됐다. 결국 AIDS는 HIV에 의한 면역체계의 파괴와 HlV감염으로 인한 장기의 기능장애에 기인한다. 이때 HIV의 표적은 CD-4림프구 단핵구 내식세포 단핵유래세포 등이다.
일반적으로 어떤 질병이 유지되려면 새로운 세포에 대한 계속적인 감염이 필요하다. 따라서 생체내에서 HIV의 증식을 효과적으로 방해한다면 질병의 진행을 저지할 수 있을 것이다.
학자들로부터 큰 주목을 받아 온 약제로는 HIV의 역전사효소(reverse transcriptase, RT) 억제제를 꼽을 수 있다.
HIV감염의 메커니즘에 관한 지식이 쌓여감에 따라 많은 중요한 사실들이 새로 알려졌다. 즉 감염초기에 일시적으로 증가한 HIV는 곧 숙주(감염된 사람)의 반격을 받는다. 다시 말하면 우리 몸의 면역기능에 밀려 (이때 세포면역의 '왕'인 T림프구와 중화항체가 주로 활약한다) HIV는 급격히 감소된다. 이로써 감염자는 아무런 증상없이 수년을 지내게 된다. 이 시기를 보통 무증상기혹은 잠복기라고 부르는데, 그 기간은 평균 10년 정도다.
그러나 세월이 흐름에 따라 세포면역을 주도했던 CD-4림프구가 차츰 파괴돼 줄어들고, 반대로 HIV 숫자는 점차로 증가된다. 이는 곧 면역기능의 상실을 뜻한다. 그 결과로 기회감염과 악성종양 등이 생기게 되는데 이 마지막 단계를 AIDS라 부르고 있다.
다른 여러 질병에서와 마찬가지로 AIDS의 경우에도 질병의 마지막 단계에서 손을 쓰기 시작하면 효과적인 치료를 기대할 수 없다. 따라서 무증상 상태의 감염자를 조기에 발견해 항바이러스요법을 시행하는 것이 무엇보다 중요하다.
AZT의 약효와 부작용
AIDS를 치료하는 약으로 가장 널리 알려진 것은 AZT(azidothymidine)다. 지도부딘(zidovudin, ZDV)이라고도 불리는 이 약은 전형적인 HIV의 역전사효소 억제제로 피리미딘 뉴클레오사이드(pyrimidine nucleoside)의 유도물질이다. 이를테면 뉴클레오사이드 유사물질인 셈이다. 이 약은 시험관 내(in Vitro)에서 HIV-1의 복제를 억제하는 기능을 보여주었는데 임상적으로도 그 효과가 증명된 상태다.
처음엔 항암제로 개발된(1964년) AZT는 인간 세포내에 들어가면 HIV를 잡는 물질(5'triphosphate)을 내놓는데 이것이 HIV의 역전사효소 억제제로 작용한다. 역전사효소는 HIV의 복제과정에서 필수적인 효소이기 때문에 AZT 디데옥시뉴클레오사이드(dideoxynucleoside) 등은 이 효소의 억제를 통해 항바이러스 작용을 발휘한다.
초기 실험에서 AIDS환자에 이 약제를 사용한 경우 CD-4림프구의 증가. 바이러스 부하의 감소, 전신증상의 호전, 사망률 및 기회감염의 감소가 뚜렷이 나타났다. 하지만 이 초기실험에서 사용한 만큼 환자에게 AZT를 제공할 경우 많은 부작용이 발생하기 때문에 현재는 훨씬 감량해 AZT 1백㎎을 매 4시간 마다(또는 밤중에 한번은 생략해 하루에 5백㎎만) 투여하고 있다. 이 약은 입을 통해 복용해도 잘 흡수된다.
최근에는 특별한 증상을 보이지 않는 환자와 경미한 증상을 나타내는 환자에게 AZT를 사용하였을 때 심한 HIV질환으로의 진행을 지연시키는 효과가 있음이 밝혀져 CD-4 림프구수가 5백개 이하인 경우에도 처방되고 있다. 그러나 최근 다른 연구결과에 따르면, 수명연장의 효과는 인정할 수 없으며 단지 AIDS로의 진행만을 지연시킨다는 보고도 있다. 만일 이 조사가 옳다면 무증상적인 기간(정상 생활이 어느 정도 이뤄지는 시기)이 길어짐을 뜻한다. 따라서 설령 수명연장 효과가 없다 하더라도 환자의 삶의 질에 있어서는 훨씬 향상됨을 의미하기 때문에 AZT가 긍정적인 효과를 준다고 볼 수 있다.
하지만 AZT는 독성이 크기 때문에 투여시(특히 AIDS 말기일 때)신중을 요한다. 골수에 대한 독성이 가장 흔하게 나타나는데 복용 초기부터 빈혈을 유발할 수 있다. 과립구나 혈소판의 감소도 나타난다. 또 AZT의 부작용으로 근육통도 흔하며, 장기 복용자에게 근병증이 나타나기도 한다.
또 1년이상 AZT를 사용한 환자의 몸에서 분리된 HIV는 이 약제에 대한 감수성이 떨어져 있다. 즉 AZT 공세 쯤은 능히 견델 수 있게끔 HIV자체의 방어력이 강화되는 것이다. 이것은 아마도 역전사효소의 돌연변이에 기인한 것으로 생각된다. 그러나 AZT내성을 갖게된 HIV라 할지라도 또 하나의 역전사효소 억제제인 디데옥시뉴클레오사이드에 대하여는 여전히 약한 면모를 보인다.
AZT의 '사촌들', 즉 10여개 이상의 디데옥시뉴클레오사이드 유사물질들이 시험관내에서 항(抗)HIV능력을 보여주고 있다. 그중 ddC ddA ddl d4T 아지도(azido)-ddU 등은 이미 임상실험에 들어가 있다.
그중 ddC는 이미 임상시험을 거쳐 그 약효와 부작용이 대부분 규명된 상태다. 이 약은 바이러스 부하의 감소, 높은 생활성도(bioavailability)를 보일 뿐더러 골수에 대한 독성이 적다. 그러나 말초 신경병증을 일으키는 것이 치명적인 부작용으로 알려져 있다. 현재 ddC는 AZT와 병합사용하는 것이 연구되고 있다.
한편 ddl는 경구투여로 잘 흡수되고 상당히 진행된 AIDS 환자에게 투여해도 항바이러스 효과를 보인다. 또 세포내 반감기가 AZT보다 더 길고 골수독성이 적은 것이 장점이다. 그리고 HIV가 AZT에 대해 내성을 보이는 경우에도 여전히 ddI에는 감수성을 보인다는 점도 이 약을 돋보이게 한다. 그러나 산에 약해 경구투여시 버퍼를 같이 사용해야 된다는 점이 ddI의 보급확대를 가로막고 있다.
ddl는 1991년 10월 AZT에 이어 두번째로 HIV치료제로 허가된 역전사효소 억제제다. 현재는 어떤 이유로 AZT를 사용할 수 없거나 AZT의 부작용 때문에 임상적으로나 면역학적으로 병세가 악화된 경우에만 ddl가 처방된다. 이 약은 성인이나 어린이HIV감염자에게 바이러스 부하를 줄여주고 면역학적 호전(CD-4림프구의 증가 등)을 가져다 준다.
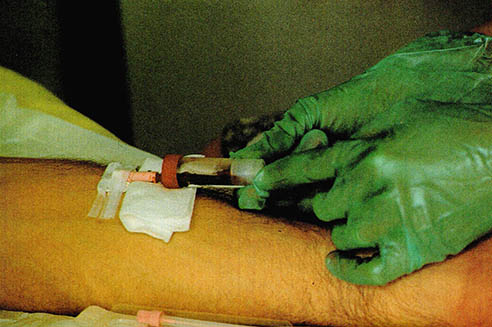
병합치료가 효과적
이번에는 비(非)뉴클레오사이드계 AIDS치료제에 대해 알아보자. 최근에 각광받고 있는 비 뉴클레오사이드계 역전사효소 억제제는 강력한 항 HIV활성에 비해 독성은 매우 낮은 장점을 가지고 있다. 여기에는 TIBO 유도체, Bl-RG-587, 피리돈 유도체, BHAPs 등이 속한다. 이 약제들은 HIV-1의 역전사효소를 억제하는 것으로 생각되며, 낮은 독성을 보여 현재 상당한 기대를 받고 있으나, 사용한지 6~12주만 돼도 약계 내성이 생기기 때문에 다른 약제와의 병합사용이 유용할 것으로 생각된다.
한편 BIV-1 복제에 관여하는 복합적인 조절 유전자기능에 대한 이해가 깊어짐에 다라 Tat를 억제하는 새로운 종류의 약제가 선보이게 되었다. 여기서 Tat는 HIV-1의 유전자 발현을 증가시키며, 전사과정에서도 중요한 역할을 하는 단백질이다.
역전사효소 억제제의 약효가 알려진 이후 HIV의 특이한 유전자를 억제하는 약물에 대한 관심이 부쩍 높아지기 시작했다. 그 결과 HIV-1의 단백분해효소(protease)억제제가 개발됐다. 성숙한 바이러스가 형성되려면 HIV-1의 단백분해효소가 활성화되어야 한다. 따라서 HIV-1의 단백분해효소 부위에 돌연변이가 생기게 하면 미숙한 바이러스입자가 나타난다.
단독으로 약제를 사용할 때 흔히 경험하는 약제내성의 출현과 치료 실패, 그리고 심한 독성을 방지하기 위해 AIDS치료시 병합요법을 적극 시도하고 있다. 병합요법의 이점으로는 항바이러스효과의 증강, 저용량의 사용으로 인한 독성 감소, 약제 내성변이 바이러스의 출현예방 등이 있다. 현재 많은 종류의 약제들의 병합이 이뤄지고 있다. 실제로 AZT ddl 알파인터페론 ddC 등을 병합사용했을 때 좋은 결과가 나오고 있다. 또 단백분해효소 억제제와 AZT ddC 알파 인터페론의 병합투여도 시도되고 있다.
과거에 인류의 가장 커다란 위협이 되어왔던 무서운 전염병, 예컨대 두창(천연두) 소아마비 흥역 등은 이제 완전히 없어졌거나 거의 소멸되어 잊혀져가는 병이 되었다. 이것은 무엇보다도 이들 질병에 유효한 예방백신이 개발되었기 때문이다. AIDS라는 새로운 전염병이 나타났을 때 사람들이 이러한 백신의 출현을 기대한 것은 무리가 아니다. 그러나 이 경우 우리가 당면한 도전은 유례가 없는 것이다.
바이러스의 당단백에 관심집중돼
우선 사람의 레트로바이러스(HIV는 레트로바이러스의 일종이다) 감염과 그에 대한 백신개발 경험이 거의 없었다. 더구나 이 바이러스는 자연적인 면역방어망을 뚫고 들어와 오랜 잠복기를 지난 후에야 발병하는 치명적인 병원체이다. 이처럼 면역 방어망을 잘 회피하고 엄청난 돌연변이율을 보이는 레트로바이러스는 자체의 유전자를 사람의 DNA에 통합하여 잠복상태로 존재하며, 바이러스 감염에 중추적인 면역기능을 담당하는 세포인 CD-4림프구를 파괴하여 궁극적으로 사람의 면역체계를 무력화하는 독특한 특성이 있다. AIDS 백신 개발에서 가장 중요한 부분은 바이러스 외피의 당단백(glycoprotein)이다. 이 부분은 아미노산의 변이가 매우 심하다. 따라서 바이러스마다 다른 이 부분에 대하여 어떻게 하면 모든 경우에 들을 수 있는 항원을 찾아내 백신에 이용하느냐 하는 것이 어려운 문제다.
또 바이러스의 어느 부분이 방어에 관여하는 항원을 가지고 있느냐 하는 문제 뿐 아니라, 사람의 주요한 두 면역반응(세포성과 체액성)중에서 방어상 더 큰 역할을 하는 것도 밝혀야 한다. 종래에는 바이러스 외피의 당단백중 V3 영역에 미치는 중화항체의 역할에 대해 특히 주목하였으나, 최근에는 T림프구에 의한 세포성 면역의 형성이 바이러스 방어전선에서 중추적 역할을 하고 중화항체 같은 체액성 면역은 단지 이것을 돕는 역할을 하는 것이 아닌가 생각하고 있다.
어쨌든 유효한 백신이 되기 위하여는 레트로바이러스의 광범위한 항원변이를 모두 방어하여야 한다. 또 실제로 HIV는 외따로 떨어져 있는 상태(세포안이 아닌), 즉 유리된 바이러스가 아닌 세포내(림프구 단핵구 내)에 들어있는 상태로 사람의 몸속으로 침투하기 때문에 중화항체처럼 세포내로 들어갈 수 없는 '무기'는 HIV와의 실제 전투상황에서 별 효과가 없을 것이다. 또 대부분의 HIV는 직접 핏속으로 들어오지 않고 성관계에서 처럼 사람의 점막을 통하여 침입하기 때문에 침투로의 입구가 되는 점막에서 HIV의 침입을 저지할 수 있는 면역이 형성되어야 할 것이다. 물론 이러한 백신은 무엇보다 안전성이 보장되어야 하며, 한번 백신을 맞으면 가능한 한 오랜기간 면역이 유지되는 것이 유리함은 물론이다.
실험동물이 태부족해
한편 유력한 백신후보를 미리 시험해 볼 수 있는 실험동물이 매우 적은 것이 큰 장애가 되어 왔다. 희귀한 침팬지외에도 다행히 최근 돼지꼬리 원숭이(pigtail macaque)가 HIV에 감염될 수 있음이 알려져 백신연구에 큰 도움을 줄 것으로 기대된다. 과거에 백신을 만들 때 사용하던 방법, 즉 죽은 바이러스를 사용하거나 그 독성을 약화시킨 것을 사용하는 것은 안전성문제 때문에 이제는 채택되지 않는다. 따라서 유전공학적인 방법을 이용하여 바이러스의 일부 주요성분(유전자재조합 단백 등)을 얻어 백신으로 사용하는 방법이 주로 시도되고 있다.
현재 세계 여러 나라에서 많은 노력이 경주되고 있지만, 아직은 안전성과 효과면에서 만족할 만한 백신은 없다. 몇가지 중요한 진전을 소개하면 이렇다.
침팬지는 돼지꼬리 원숭이를 제외하고는, HIV-1에 급성 및 지속적 감염을 일으키는 유일한 동물이다. 따라서 침팬지를 이용해 HIV-1에 대항하는 AIDS백신을 제조할 수 있다. 유전자 재조합법으로 만든 외피백신을 침팬지에 주입했을 때 돼지의 몸안에 중화항체가 형성됐다. 이는 외피백신이 HIV에 대한 방어 능력을 갖추고 있음을 뜻한다. 또 HIV-1에 걸린 사람의 면역글로블린이나 그 바이러스의 외피 성분을 이용해 만든 단클론항체를 침팬지에게 제공했더니 HIV에 대한 면역이 형성됐다(수동면역). 이 침팬지들은 나중에 HIV에 실제로 노출됐지만 거의 감염되지 않았다. 미국과 유럽에서 70마리의 침팬지를 HIV-1항원으로 면역시켰는데 그 중 12마리에서 중화항체가 나타났다. 이 침팬지들의 몸 안에 HIV를 넣어 주었을 때, 7마리에서 HIV의 감염이 예방됐다. HIV를 이겨낸 7마리의 침팬지는 거의 완전한 방어면역을 획득하고 있었다. 일시적인 감염이나 침입조차도 일어나지 않는 이른바 멸균면역(sterilizing immunity)상태를 보인 것이다.
짧은꼬리 원숭이(macaque)는 HIV-2에 의하여 감염되지만 그 자신이 AIDS로 고통받지는 않는다. 이 짧은꼬리원숭이에서 분리한 HIV-2를 이용해 만든 실험적 백신은 AIDS관련 학자들의 관심을 끌고 있다. 외부에서 같은 종류의 유리(세포밖에 있는)바이러스를 짧은꼬리원숭이에 소량주사하였을 때 100%의 방어능력을 보였기 때문이다.
SIV는 몇가지 종의 아프리카 원숭이에서 자연적으로 발생하는 무해한 바이러스다. 그러나 SIV중 어떤 종류를 자연 숙주가 아닌 인도 짧은꼬리원숭이에 주사하면 사람의 AIDS와 비슷한 원숭이의 면역 결핍증상을 일으킨다. 따라서 이 SIV는 원숭이 AIDS의 원인병원체인데, 사람의 HIV-2와 매우 가깝다. 짧은꼬리 원숭이에 활성을 없앤 SIV백신을 접종시켰더니 SIV의 침입을 성공적으로 막아 내었다. 이러한 방어는 비교적 단기간(1년이내)에 그쳤으나, 감염을 완전히 막아내었고, 외피 아미노산이 11% 정도 차이가 나는 다른 종류의 바이러스에도 유효하였다. 그러나 SIV백신을 정맥에 주사해 HIV의 방어에 성공한 경우라도, 점막을 통한 HIV의 침입을 막는 데는 실패하였다. 유전적 조작을 통해 만든 SIV백신을 짧은꼬리원숭이에 주사해 면역시킨 뒤, 독성이 강한 SIV를 다시 정맥주사한 경우, 백신을 맞은 원숭이는 성공적으로 강력한 도전자의 침입을 방어하거나 혹은 감염되더라도 오랫동안 건강한 상태로 남아있음이 관찰되었다. 이 경우에도 바이러스에 대항하는 항체보다는 감염된 세포에 타격을 가하는 세포성 면역이 방어에 더 기여한 것으로 생각된다. 유전공학적 방법으로 만든 현대적인 HIV 백신으로는 아직 이 모델에서 성공적인 결과를 내지 못하였다. 그러나 독성이 약한 SIV백신을 이용한 모델에서는 동종의 바이러스에 대한 방어면역을 유도하는 데 성공하였다.
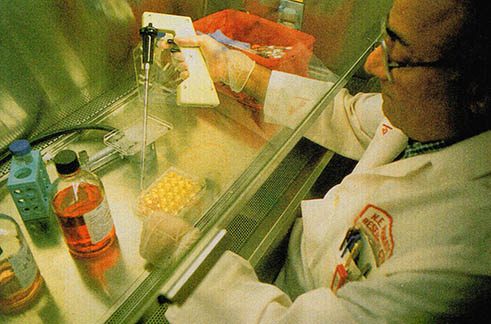
12종류 이상의 맥신 시험중
감염되지 않은 사람에서 실험적 HIV백신의 안전성과 효과를 알아내기 위한 임상시험이 현재 활발히 진행되고 있다. 대체로 12종류 이상의 백신에 대한 임상시험이 시행중이다. 여기에는 유전자 재조합법으로 만든 외피당단백 gp160 gp120을 여러 바이러스 세포 효모 등을 이용하여 발현시킨 백신들이 포함되어 있다. 또 Pl7 P24 등 핵심부 단백(효모내 혹은 펩티드 형태)을 이용해 제조한 백신, 재조합 gp160과 살아있는 폭스바이러스 벡터 등을 이용해 만든 백신도 나와 있다. 이들 백신은 대체로 안전하며 면역성이 있다. 이들은 같은 종류의 바이러스에 대하여 매우 낮은 역가의 중화항체를 형성하였다. 또 T림프구에 의한 세포면역도 관찰되었다. 대개의 백신은 CD-4 활성은 있었으나 세포독성 림프구인 CD-8의 활성은 나타나지 않았다. 두 종류의 gp160백신은 침팬지를 HIV로부터 보호하는데 성공했다.
아직 감염되지 않은 사람에 대한 백신은 극히 초보단계의 수준(안전성과 면역성에서)을 보여주는데 머무르고 있다. 또 동물에서도 극히 인공적이고 이상화된 상황에서만 제한적으로 방어면역 형성을 확인하는 단계에 있을 뿐이다. 따라서 엄청난 변이의 능력을 특징으로 하고, 주사가 아닌 성관계가 주요 감염경로인 AIDS바이러스를 막을 수 있는 만족스러운 백신의 개발이나 실용화는 수년 내에는 어려울 것으로 보인다. 빨라야 21세기(몇년 안 남았기는 하지만)이후에 가서야 가능할 것으로 생각된다.