제목 │HDAC6 선택적 저해제를 통한 다발성 골수종의 보르테조밉 내성 극복
교신저자 │ 권소희 연세대 약학과 교수는 후성유전학 및 염색질 생물학 연구실을 운영하고 있다. 유전자의 유지와 발현에 중요한 역할을 하는 단백질과 그 기전을 연구한다. 이를 통해 암을 비롯한 유전질환, 신경계질환 등 난치성 질환을 치료할 방법을 개발하고 있다.
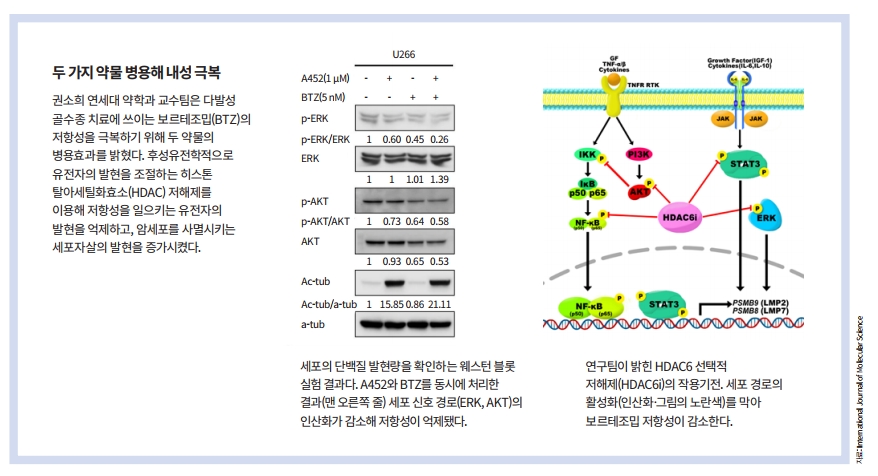
초록 │ 다발성 골수종을 치료하기 위한 표준 치료제는 보르테조밉이지만, 여전히 재발과 내성 문제가 있다. 본 논문에서는 히스톤 탈아세틸화효소(HDAC)6 억제제인 A452가 다발성 골수종에서 보르테조밉 내성을 극복할 수 있는지 알아봤다. 보르테조밉에 내성을 가진 다발성 골수종 세포에 HDAC6 선택적 억제제를 처리하자 내성과 관련된 세포신호 전달 체계의 활성이 떨어졌다. 또 보르테조밉, 카르필조밉과 함께 사용할 경우 병용효과에 의해 내성은 더욱 감소하고, 암세포의 성장률이 떨어지고 세포자살이 유도됐다. 이번 연구는 보르테조밉에 내성을 가진 다발성 골수종을 치료하기 위한 후보군으로서 HDAC6 억제제의 가능성을 보여준다.
다발성 골수종은 혈액암의 한 종류로, 백혈구의 일종인 형질세포(plasma cell)가 암세포로 변해 골수에서 비정상적으로 증식할 때 발생합니다. 혈액암 중에서 백혈병 다음으로 흔합니다. 다발성 골수종 환자는 지속해서 통증을 느낍니다. 빈혈과 골절, 과칼슘혈증을 동반하기도 하고, 면역 기능이 떨어지며 신부전까지 발생할 수 있습니다.
다발성 골수종 항암제의 치명적 단점
다발성 골수종을 치료하기 위해서는 주로 항암화학치료가 시행되고 있습니다. 대표적인 항암제는 보르테조밉(bortezomib·BTZ)입니다. BTZ는 단백질분해효소 억제제(PI)의 일종으로, 세포질 내 단백질을 분해하는 유비퀴틴-프로테아좀 시스템(UPS)의 작용을 억제합니다. 그 결과, 세포 내에 비정상적으로 단백질을 축적시키고 소포체의 스트레스를 증가시킵니다. 정상적인 세포라면 새로운 단백질 합성을 억제해 이를 극복하겠지만, 암세포는 생장을 억제하지 못하기에 소포체 스트레스에 취약합니다. 결국 쌓이는 스트레스로 암세포가 세포자살에 이르도록 합니다. 이외에도 다양한 요인에 영향을 미쳐 암세포의 세포자살을 촉진하거나 성장을 억제할 수 있습니다.
물론 단점도 있습니다. BTZ의 약효가 점차 떨어져 저항성을 보이다 다발성 골수종이 재발하는 경우가 있습니다. 저항성을 극복하기 위해서 BTZ와 유사한 새로운 PI가 연구되고 있습니다. 2세대 PI로 꼽히는 카르필조밉(carfilzomib·CFZ)이 대표적이지만, 아직 임상이 진행되는 단계입니다. 그 밖에도 여러 PI가 개발되고 있지만, BTZ처럼 의료 현장에서 사용하는 PI는 아직 없습니다. 이번 논문탐독에서는 기존 약물과 새롭게 개발한 약물의 작용기전을 기반으로 두 가지 약물을 함께 썼을 때 나타나는 효능을 세포 내에서 확인하는 연구를 소개합니다.
후성유전학의 암 정복 가능성
이번에 소개할 논문에서는 다발성 골수종을 앓는 환자에게 BTZ 저항성이 나타나는 원인에 주목했습니다. BTZ는 단백질을 분해하는 프로테아좀 단위체 중 β5와 β1에 결합해 활성을 억제합니다. BTZ에 저항성을 보이는 다발성 골수종 환자의 세포를 보면, β5와 β1 단위체 수가 증가하는 현상을 관찰할 수 있습니다. 동시에 두 단위체를 대체할 수 있는 면역계 프로테아좀(immune-proteasome)의 발현이 늘어남도 확인할 수 있습니다. ‘LMP2’와 ‘LMP7’이라는 단백질인데, 이들이 β5와 β1을 대체해 BTZ와 결합하면서 BTZ의 효과를 떨어뜨리는 저항성이 발생합니다.
최근 주목받고 있는 다발성 골수종 치료 전략은 후성유전학적 조절입니다. 후성유전학은 세포 내에서 DNA 염기 서열을 바꾸지 않고 히스톤 단백질을 변형하는 등 유전자 발현에 영향을 주는 변화들을 의미합니다.
이 과정에 관여하는 히스톤 탈아세틸화효소(HDAC) 저해제는 좋은 항암제로 쓸 수 있습니다. 처음 개발된 HDAC 저해제인 SAHA(혹은 vorinostat)는 여러 암세포에 효과적인 선택적 저해제로 사용할 수 있다는 사실이 검증돼 미국 식품의약국(FDA)의 승인을 받았습니다. 임상 연구에 따르면, 다발성 골수종이 재발한 환자에게 BTZ과 HDAC 저해제를 함께 처리할 경우 병용(시너지)효과가 있었습니다.
하지만 이 연구에도 한계가 있습니다. 해당 저해제들은 특정 HDAC만 억제하는 것이 아니라 다수의 HDAC를 억제합니다. 자연히 세포 독성이 증가하고 정상 세포도 큰 영향을 받는 부작용이 있습니다. 이를 줄이기 위해서 몇몇 연구진은 HDAC를 선택적으로 억제하는 저해제를 개발하고 있습니다. 이 논문에서는 HDAC6에 선택적으로 결합해 억제하는 저해제인 ‘A452’와 BTZ, 또는 CFZ의 병용 효과를 확인했습니다.
단백질 경로 탐색해 병용효과 관찰
연구팀은 최근에 합성한 HDAC6 선택적 저해제인 A452가 BTZ 또는 CFZ과 병용효과가 있을 것으로 예상했습니다. 이를 입증하기 위해서는 각 약물의 작용기전이 다발성 골수종의 저항성을 효과적으로 억제하는지 검증해야 합니다.
기존에 밝혀진 연구에 따르면, BTZ의 효능을 떨어뜨리는 저항성 인자 LMP2와 LMP7의 발현과 관련 있는 신호전달경로는 NF-κB와 JAK/STAT입니다. 연구팀은 BTZ에 저항을 가진 다발성 골수종 환자의 세포와 유사한 후성유전학적 변화가 있는 세포를 활용해 실험했습니다. A452와 BTZ 또는 CFZ를 저항성이 있는 다발성 골수종 세포와 없는 세포에 각각 처리한 뒤 단백질의 발현량을 확인했습니다. 그 결과 약물을 조합해 쓰면 이들 저항성 인자를 효과적으로 억제할 수 있음을 확인했습니다.
이때 사용한 실험 방법은 ‘웨스턴 블롯(Western Blot)’입니다. 특정 단백질과 결합하는 항체에 표지를 달아 그 발현량을 확인하는 실험 기술입니다. 항암제를 개발할 때뿐만 아니라 단백질의 새로운 기능을 찾거나 질병의 원인을 밝힐 때 등 대부분의 생명과학 연구에 쓰이고 있습니다.
웨스턴 블롯의 실험 결과는 검은색 밴드의 굵기로 알 수 있습니다. 확인하고자 하는 단백질의 양이 많다면 밴드는 굵어집니다. 웨스턴 블롯의 실험 결과를 해석하는 것도 간단합니다. 밴드는 보통 가로로 배열됩니다. 맨 왼쪽에는 양을 확인한 단백질의 이름이, 위쪽에는 각 밴드에 해당하는 실험 조건이 쓰여 있습니다. 정량적인 비교가 필요한 경우에는 프로그램을 이용해 밴드의 진하기를 수치화한 그래프가 함께 쓰이기도 합니다.
이어 연구팀은 약물의 효능을 본격적으로 확인하기 위해 세포자살 또는 생존 관련 신호전달경로인 ERK와 AKT에서 약물이 어떤 기능을 하는지 알아봤습니다. 저항성이 있는 세포와 없는 세포에 조합된 약물을 처리해 웨스턴 블롯을 통해 확인한 결과 ERK와 AKT 경로가 효과적으로 억제된다는 사실을 확인했습니다.
세포자살 효과를 확인하기 위한 과정도 거쳤습니다. 여기에는 유세포 분석(FACS)이라는 기술이 쓰였습니다. 먼저 세포자살과 관련된 단백질을 형광 염색합니다. 이 단백질은 세포자살 과정에서 세포 표면에 특이적으로 나타나기 때문에 정상 세포일 경우에는 염색이 되지 않습니다. 이후 염색된 세포를 좁은 통로로 흘려보냅니다. 그리고 분석 기기로 염색된 세포를 일일이 세어 결과를 확인합니다. 연구 결과 조합된 약물이 효과적으로 다발성 골수종의 세포자살을 증가시킨다는 사실까지 확인했습니다.
새로운 약물을 개발하고 그 효능을 증명하는 것은 오랜 시간과 여러 단계가 필요한 과정입니다. 연구에 많은 시간과 비용을 투자하고도 사라지는 약물이 많습니다. 오히려 끝까지 살아남아 환자들에게 쓰이는 약은 소수에 불과합니다. 하지만 과학자들이 이런 도전을 계속 이어가는 이유는 단순합니다. 사람들의 생명과 건강에 가장 밀접한 연구이기 때문입니다. 현대과학은 극도로 발전했지만, 여전히 정복하지 못한 질병은 많습니다.
앞으로 치료제를 개발하고자 하는 사람들은 관련 논문을 여럿 읽어보길 추천합니다. 현재 치료제가 없는 질병은 무엇인지, 또 치료제가 있더라도 부작용을 개선해야 하는 질병은 무엇인지 알 수 있습니다. 많은 과학자가 겪은 성공담과 실패까지도 말입니다.

※필진소개.
이상우. 연세대 약학과 석·박사통합과정에 재학하고 있다. 항암제로 이용 가능한 후보 물질을 찾는 연구를 하고 있다. tkddn407@naver.com