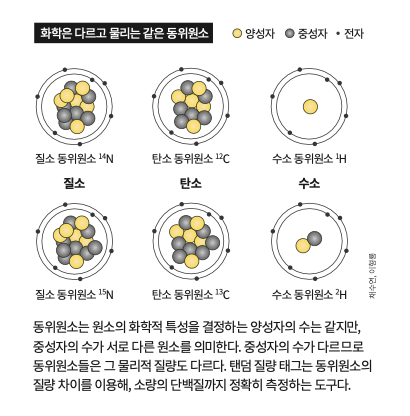
원자라는 이름은 고대 그리스어로 ‘더 이상 쪼갤 수 없는’을 뜻하는 아토모스(atomos)에서 기원했습니다. 원자는 중성자, 양성자로 이뤄진 원자핵과 그 주위의 전자로 구성되죠. 원자를 이룬 양성자의 개수에 따라 화학적 특징이 달라지며, 이를 기준으로 원자들을 분류해 원소라고 부릅니다. 원자의 화학적 특성은 양성자의 수에 의존하므로, 같은 화학적 특성의 원소로 분류돼도, 무게는 서로 다른 원자들이 존재하게 됩니다.
분자의 정체를 밝히는 열쇠, 동위원소
탄소는 6개의 양성자, 6개의 중성자와 6개의 전자로 이뤄진 12u의 12C가 존재하며, 6개의 양성자, 7개의 중성자와 6개의 전자로 이뤄진 13u의 13C도 존재합니다. 이때 12C와 13C는 화학적 특성은 같지만 그 질량이 다르므로, 동위원소라고 불립니다. 탄소 동위원소 12C, 탄소 동위원소 13C 식으로 말이죠.
이런 동위원소들은 모든 원소에 있습니다. 다만 자연계에서 각각의 존재 비율이 다른 까닭에, 그 비율을 고려해서 평균 질량을 사용하죠. 12C의 질량은 12g이며 13C는 13g이나 자연계에서 이 두 동위원소의 비율이 98.9%, 1.1%이기에 탄소의 평균 원자량은 12.011u가 됩니다. 더 복잡한 물 분자(H2O)는 2개의 수소와 1개의 산소로 이뤄져 평균 질량이 18.016u입니다.
하지만 실제로는 수소의 동위원소(1H, 2H)와 산소의 동위원소(16O, 17O, 18O)가 짝을 이뤄, 18.011, 19.017 등 질량이 서로 다른 단일 동위원소 질량의 물 분자가 99.73%, 0.06%의 비율로 존재합니다. 즉 우리는 무게가 비슷한 분자들이 섞여있어도 동위원소의 비율(동위원소 패턴)을 이용해서 정확히 어떤 분자인지 유추해낼 수 있죠.
질량분석법은 전하를 띠는 물질인 이온의 질량 대 전하비(m/z) 및 이온에 있는 동위원소의 비율을 측정해 이온의 종류와 그 양을 분석하는 실험 기법입니다. 발생한 이온을 살펴보는 방식에 따라 검출법도 달라집니다. 질량분석기로 형성된 전구체 이온(Precursor ion)을 살펴보면 질량분석법(MS), 전구체 이온을 힘으로 쪼개 파편 이온(Product ion 혹은 Fragment ion)을 살펴보면 탠덤 질량분석법(MS/MS)이라고 부릅니다.
전체는 같아도 부분이 다르다
그렇다면 왜 많은 과학자는 질량분석기 측정법 중 탠덤 질량분석을 사용할까요? 많은 이유가 있지만, 가장 큰 목적은 형성된 이온의 분자 구조에 따라서 서로 다른 패턴 이온이 발생하는 원리를 이용해 물질을 분리, 분석하는 것입니다.
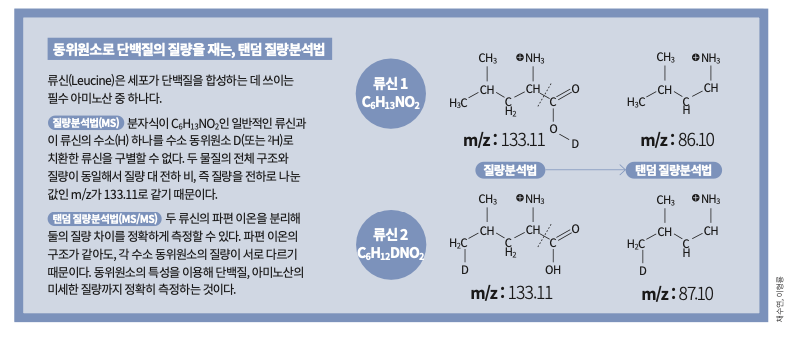
가령 아미노산 중에서 둘 다 분자식이 C6H13NO2로 동일하고 질량도 동일한데, 구조만 다른 류신(Leucine)과 이소류신(Isoleucine)을 각각 측정한다고 생각해봅시다. 질량분석기는 단일 동위원소 질량을 전하로 나눈 값인 m/z을 보여줍니다. 류신과 이소류신은 전하가 각각 1개입니다. 그래서 전구체 이온만으론 둘의 m/z도 132.11으로 동일해서, 두 아미노산 중 무엇이 존재하는지 제대로 알기 어렵습니다. 반면 탠덤 질량분석법은 전구체 이온의 구조에 따라 생성되는 파편 이온이 다르기 때문에, 시료에 두 물질 중 무엇이 존재하는지 바로 알 수 있죠.
그러면 분자식이 C6H13NO2인 류신과 여기서 수소 원소 하나가 수소 동위원소 D(또는 2H)로 치환된 류신 C6H12DNO2는 어떻게 측정될까요? 이 두 물질도 구조가 같아서 질량분석법에선 m/z 값이 모두 133.11입니다. 반면 탠덤 질량분석법은 두 류신의 파편 이온 속 동위원소의 질량 차를 이용합니다. 각 파편 이온의 m/z는 86.1, 87.1로 측정됩니다. 즉 우리는 탠덤 질량분석으로 이 둘의 혼합 용액에서도 그 구성 비율을 파악할 수 있죠.
이번 주제 논문은 단백체 정량분석에서 가장 많이 쓰는 동위원소 표지법 중 하나인 ‘탠덤 질량 태그(Tandem Mass Tags, TMTs-labeling)’의 시초입니다. 구조와 질량이 같지만 동위원소의 위치가 다른 탠덤 질량 태그인 두 물질 TMTa, TMTb를 이용해, 단백질 정량분석법을 혁신한 논문이죠. 구조는 같아도 질량이 다른 동위원소들의 특성이 여기서 중요한 역할을 합니다.
이 논문이 제안한 두 종류의 TMT는 파편화 부분, 파편화를 증가시키는 부분, TMT 분자의 전체 질량을 맞추는 부분, 펩타이드의 N-말단과 화학반응을 하는 부분으로 구성됩니다. 펩타이드의 N-말단과 TMT 분자의 해당 부분이 화학반응을 일으켜, 펩타이드를 각각의 TMTa/TMTb로 표지합니다. 이 TMTa/TMTb는 구조가 동일한 물질이므로 그 전구체 이온들도 같습니다. 즉 질량분석법으로 동일한 양의 펩타이드-TMTa와 펩타이드-TMTb를 혼합해 분석하면, 이 둘을 따로 분석할 때보다 펩타이드-TMT에 해당하는 m/z에서 신호가 2배로 커지죠.
펩타이드-TMTa, 펩타이드-TMTb가 섞인 이 펩타이드-TMT 이온으로 탠덤 질량분석을 하면, 각각의 동위원소에 따라 파편화 이온의 질량이 달라집니다. 즉 우리는 먼저 펩타이드-TMTa/TMTb를 혼합해 질량분석법에서 신호의 세기를 더 키웁니다. 이렇게 신호가 커진 펩타이드-TMT 이온을 탠덤 질량분석하면 시료에서 펩타이드-TMTa, b의 정확한 비율을 얻게 됩니다. 구조는 같고 질량이 다른 동위원소의 특성을 이용해 혼합물질의 신호 자체를 키우고, 훨씬 미세한 질량까지 측정하는 것이죠.
단백체학 분야의 획기적 발전 이끌 것
이 논문은 여러 종류의 펩타이드를 정량분석했습니다. 그중특정한 물질을 선택적으로 분석하기 어려운 용해물(여러 DNA, 단백질, 생분자 물질 등이 섞인 용액)에 펩타이드-TMTa와 펩타이드-TMTb를의 비율로 더한 정량분석도 있었죠. 질량분석법과 달리, 탠덤 질량분석법은 시료의 신호 세기를 키워 TMTa, TMTb의 파편화 이온을 39.3%, 60.7%로 각각 검출했습니다. 분석이 매우 어려운 복잡한 시료에서도 탠덤 질량 태그로 표지한 펩타이드들을 훨씬 정확, 정밀하게 분석했죠.
현재 정량분석에 널리 쓰이는 TMT는 가장 흔한 원소 중 하나인 수소는 물론 탄소, 산소, 질소의 동위원소까지 이용해 최대 18개의 동위원소를 표지하는 수준으로 크게 발전했습니다.
18개의 TMT로 시료를 표지하고 이 시료들을 혼합, 분석하면 아주 소량의 펩타이드도 정확히 측정할 수 있습니다. 시료 1개엔 펩타이드가 단 1%만 있어도, 서로 다른 동위원소가 표지된 시료 18개를 섞으면 신호가 18배 이상 증가해서죠. 펩타이드, 단백체 정량분석의 정밀도를 획기적으로 높인 원리입니다.
따라서 개개인의 신체 특성을 보여주는 중요 물질인 단백체에 관한 의학, 약학 등을 연구할 때 TMT처럼 동위원소 치환법을 이용한 탠덤 질량분석법은 반드시 필요한 연구 기법입니다.
치료, 완치가 어려운 대표적인 질환인 암은 암 유발 요인, 치료 약물에 대한 저항성 요인 등 여러 생체요인이 치료에 영향을 미칩니다. 단백질도 이런 요인들과 관계가 깊다고 알려졌죠. TMT를 이용한 단백체 정량분석으로 암세포에서 다량 발현되는 단백질의 종류와 그 구체적 역할 등을 많이 규명했고, 이를 바탕으로 해당 단백질을 겨냥한 항암제도 계속 개발 중입니다.
이처럼 단백체 정량분석은 생명 연장과 질병 극복을 달성하기 위한 현대 의학, 약학의 핵심적인 연구 수단으로 자리잡았기에, 이 논문의 의의도 계속 커질 것이라고 봅니다.