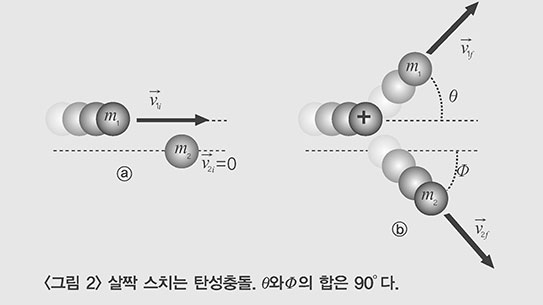
일과 에너지는 서로 순환한다. 이때 에너지의 양은 보존되지만 그 형태는 끊임없이 변한다. 이러한 에너지의 변신은 여러 가지 자연현상으로 나타난다.
Q1
다음 제시문을 읽고 물음에 답하라.
(가) 질량이 같은 물질을 가열할 때 어떤 물질은 열을 조금만 가해도 온도가 쉽게 올라가지만, 어떤 물질은 같은 열을 가해도 온도가 잘 오르지 않는다. 이것은 물질에 따라 단위 온도를 변화시키는 데 필요한 열량이 다르기 때문이다. 어떤 물질 1kg의 온도를 1K 올리는 데 필요한 에너지를 그 물질의 비열이라고 하며, 단위로는 J/kg•K 또는 kcal/kg•K를 사용한다. 물체의 질량이 같으면 비열이 큰 물체일수록 같은 열량에 의한 온도 변화가 작다.
물질의 상태가 기체일 때 부피는 온도와 압력에 따라 변하므로 부피를 일정하게 유지하거나 압력을 일정하게 유지하면 비열의 값이 달라진다. 이때 기체의 부피를 일정하게 유지하면서 측정한 비열을 정적 비열, 압력을 일정하게 유지하면서 측정한 비열을 정압 비열이라고 한다.
(나) 물체가 정지하고 있더라도 물체를 구성하는 분자들은 끊임없이 운동하고 있다. 뿐만 아니라 이들은 분자 상호간에 작용하는 힘에 의한 위치에너지도 갖고 있다. 이와 같이 물체 내의 분자들이 갖는 운동에너지와 위치에너지, 분자 내부에 저장되는 에너지를 모두 합해 그 물체의 내부 에너지라고 한다. 이상기체를 이루는 분자들은 충돌할 때를 제외하고는 서로 힘을 미치지 않고 자유로이 떠돌아다니므로 위치에너지는 없고 운동에너지만 있다.
물체를 가열하거나 외부에서 물체에 일을 해주면 물체의 내부 에너지는 증가한다. 그러나 물체로부터 열을 빼앗거나 물체가 외부에 대해 일을 하면 물체의 내부 에너지는 감소한다. 외부에서 물체에 Q의 열량을 가할 때 물체의 내부 에너지 변화량 △U와 물체가 외부에 한 일 W는 Q=△U+W를 만족한다. 이것은 에너지보존 법칙으로 열역학의 제 1법칙이다. 이 법칙은 에너지가 한 형태에서 다른 형태로 전환될 수 있지만 총량은 항상 일정하게 보존됨을 의미한다.
(다) 기체의 압력과 온도가 동시에 변하는 경우에는 보일의 법칙과 샤를의 법칙을 한꺼번에 적용하면 편리하다. 즉 ‘일정량의 기체 부피는 압력에 반비례하고 절대온도에 비례한다’를 식으로 표현하면 PV/T=k(k는 비례 상수)이고 이를 보일-샤를의 법칙이라고 한다.
(라) 지표면에 있는 공기덩어리는 내부의 공기 입자가 외부에 작용하는 압력과 외부에서 공기덩어리에 작용하는 기압이 같은 상태다. 공기덩어리가 상승하면 내부의 기체 압력은 그대로지만 외부 기압이 낮아져 부피가 팽창한다. 이때 공기덩어리는 다른 에너지 공급원이 없으므로 부피를 팽창시킬 때 공기덩어리 내부의 에너지를 사용할 수밖에 없다. 공기덩어리는 팽창하면서 외부 공기에 일을 하고, 이 일의 양만큼 내부 에너지가 감소해 기온이 낮아진다. 이러한 공기덩어리의 온도 변화가 바로 단열 변화이다. 지상에 있던 공기덩어리가 상승하면 단열 팽창해 온도가 낮아지고, 상공에 있던 공기가 하강하면 단열 압축돼 온도가 높아진다.
(마) 기압은 공기의 압력이고, 압력은 단위면적에 작용하는 힘이다. 기압을 고려할 때는 흔히 밀도가 일정하고 높이에 따라 부피가 변하지 않는 공기 기둥을 생각한다. 밑면이 1m2단위면적인 공기 기둥이 지표면에 작용하는 기압을 △p, 기둥 안에 있는 공기의 밀도를 ρ, 부피를 v, 공기 기둥의 높이를 △z, 중력가속도를 g라 하면 △p=mg=(ρv)g이다. 공기 기둥의 부피는 v=밑넓이×높이=1×△z이므로 △p=mg=(ρv)g=ρg△z가 성립한다.
1) 제시문 (가)~(다)를 참고해 이상기체 A에 대한 다음 질문에 답하라.
① 단위질량의 이상기체 A에 열을 공급했을 때 내부 에너지 변화량 △U를 식으로 표현하면 △U=Cv×△T(Cv : 기체 A의 정적 비열, △T: 온도 변화량)와 같다. 그 이유를 설명하라.
② 제시문 (다)의 보일-샤를의 법칙에서 단위질량의 이상기체 A에 대한 비례상수 k를 A의 기체상수 R이라고 하면 이 기체의 정압 비열 Cp는 Cp=Cv+R과 같이 나타낸다. 그 이유를 설명하라.
2) 공기가 상승하며 단열 팽창할 때 높이 변화에 따른 건조 공기의 온도 변화량을 건조 단열 감률이라고 한다. 단위질량의 건조 공기에 대한 기체상수 Rd=287J/kg•K, 정적 비열 Cv=713J/kg•K 일 때 건조단열감률을 구하라. (단 중력가속도 g≒10m/s2이며 △P, △V가 작을 때 △P/P×△V/V≒0이다.)
전문가 클리닉
1) 비열의 정의와 보일-샤를의 법칙을 이용해 열역학 제 1법칙을 표현해 봅니다. 정적 비열과 정압 비열의 차이에 대한 이해가 핵심적인 평가 내용입니다.
2) 논제 1의 결과와 고도에 따른 압력 변화에 대한 제시문 내용을 조합해 고도에 따른 온도 변화인 단열감률 값을 구합니다. 단열변화에서는 출입한 열이 없다는 점을 유의합니다.
예시답안
1-1) 제시문 (가)에 의해 비열의 정의를 식으로 표현하면 C=Q/△T와 같다. 여기서 Q는 열에너지, △T는 온도 변화량이며 모두 단위 질량의 기체에 대한 값이다. 이 식에 열역학 제 1법칙의 Q=△U+W를 대입하면 C=△U+W/△T이다. 이때 Cv는 부피 변화가 없는 경우에 측정한 비열인 정적 비열이고, 부피 변화가 없으면 일을 하지도 받지도 않아서 W=P△V=0이므로 Cv=이다. 따라서 △U=Cv×△T이다.
1-2) ①의 결과에 의해 일반적으로 비열 C=△U+W/△T=Cv△T+P△V/△T로 표현된다. 이때 단위질량의 이상기체 A에 대하여 P×V=R×T이며, 압력이 변하지 않을 때 기체의 상태 변화는 P×(V+△V)=R×(T+△T)를 따른다. 즉 P△V=R△T (∵PV=RT)이다. 정압 비열은 압력이 변하지 않을 때 측정한 비열이므로 비열을 나타내는 앞 식에 P△V=R△T를 대입한다. 따라서 Cp=Cv△T+P△V/△T=Cv△T+R△T/△T이다.
2) 일반적인 기체의 상태 변화를 식으로 표현하면 (P+△P)(V+△V)=R(T+△T)과 같다. 이 식을 전개해 변형하면 PV1+△P/P+△V/V+△P/P×△V/V=RT(1+△T/T) 이다.
논제에 주어진 근사식을 적용해 정리하면
△P/P+△V/V=△T/T(∵PV=RT)
V△P+P△V=R△T(∵PV=RT)
∴P△V=R△T-V△P 이다.
이 식을 열역학 제 1법칙에 대입하면
Q=Cv△T+P△V=Cv△T+(R△T-V△P)이다. 단열 변화에서는 출입한 열이 없으므로 Q=0, (Cv+Rd)△T=V△P를 얻는다. 제시문 (마)에서 △p=ρg△z이므로 앞 식에 대입하면 (Cv+Rd)△T=ρVg△z이다. 고도 변화에 따른 온도 변화인 건조단열감률은 △T/△z=g/C=Cv+Rd=10/287+713=1/100(K/m)이다.
Q2
다음 제시문을 읽고 물음에 답하라.
(가) 태양은 지구에 사는 모든 생명체에게 에너지를 공급하는 중요한 별이다. 태양의 질량은 2×1030kg이고 전체의 약 70%가 수소이다. 태양 반지름은 7×105km이며, 태양과 지구 사이의 거리는 약 1.5×108km이다. 대기권 밖에서 태양광선에 수직으로 놓인 단위면적에 단위시간당 도달하는 태양복사에너지의 양은 4/9π(J/cm2•s)이다. 태양의 나이는 지구의 나이와 유사한 50억년으로 추정되며, 앞으로 50억년 정도는 에너지 생산 공장으로서의 역할을 할 것으로 예상된다.
(나) 에너지보존법칙에 의해 화학반응 전후에도 에너지는 보존돼야 하므로 발열반응에서 발생한 열량과 생성 물질의 에너지를 합한 값은 반응 물질의 에너지를 합한 값과 같아야 한다. 반응 물질 에너지의 합=생성 물질 에너지의 합+발생한 열량 반대로 흡열반응에서 반응 물질이 흡수한 열량과 반응 물질의 에너지를 합한 값은 생성 물질의 에너지를 합한 값과 같아야 한다. 반응 물질 에너지의 합+흡수한 열량=생성 물질 에너지의 합 물질은 저마다 고유한 에너지를 가지고 있다. 어떤 물질이 갖는 고유의 에너지 양을 열함량 또는 엔탈피라고 하며 H로 나타낸다. 엔탈피(H)는 절대값을 알 수 없다. 다만 화학반응이 진행됨에 따라 출입하는 열의 양으로 물질 사이의 엔탈피 변화를 알 수 있을 뿐이다. 예를 들어 수소 1몰이 수증기를 생성하는 화학반응은 H2(g)+O2(g) → H2O(g), △H≒-200kJ이다.
(다) 켈빈이나 헬름홀츠 같은 과학자는 성간 물질이 별의 인력으로 떨어지며 이때 생긴 중력 에너지 때문에 별의 내부에서도 빛이 방출된다고 생각했다. 반지름이 R0인 성간 물질이 중력 수축에 의해 반지름이 R로 수축된다면 중력 에너지의 변화량은 △E=1/2 GM2(1/R-1/R0이 된다. 특히 R0≫R라면 △E=1/2GM2/R이다. 이렇게 발생한 중력 에너지가 별의 내부 온도를 높이고 빛의 형태로 방출된다.
(라) 아인슈타인은 상대성 이론에서 질량과 에너지는 서로 전환될 수 있다는 결론을 이끌어 냈다. 그 뒤 에딩턴은 아인슈타인의 질량-에너지 등가 원리에 의해 태양 내부의 수소 원자핵이 결합하면 헬륨 원자핵으로 변하면서 막대한 에너지가 만들어진다는 사실을 밝혔다. 태양의 중심부에서는 수소 4개가 모여 1개의 헬륨이 된다. 수소의 핵은 양전하를 갖기 때문에 헬륨으로 융합되기 위해서는 강한 정전기적 반발력을 이겨내야 하며, 이러한 반응은 온도가 1000만K 이상일 때에만 일어난다. 이때 헬륨 1개의 원자량은 수소 원자 4개의 원자량보다 0.7%가 더 작다. 이와 같이 반응 후의 질량이 반응 전보다 줄어드는 현상을 질량 결손이라고 하는데, 이것은 아인슈타인의 질량-에너지 등가 원리에 의하면 질량이 에너지로 전환됨을 뜻한다. 결손 질량이 m이고 빛의 속도가 c일 때 E=mc2가 성립한다.
1) 제시문 (가)를 참조해 1초 동안 태양이 방출하는 총 에너지의 양을 구하라.
2) 제시문 (나)와 (다)를 참조해 다음 물음에 답하라.
① 옛날에는 태양이나 별의 에너지가 수소가 연소할 때 발생되는 화학 에너지라고 생각했다. 이 생각이 틀렸음을 정량적으로 증명하라. (단 수소 기체 1몰은 약 2g이다.)
② 우주 공간에 퍼져 있는 수소와 헬륨 기체는 중력에 의해 수축하면서 위치에너지가 운동에너지로 전환된다. 이는 다시 열에너지로 바뀌어 빛을 내지만 태양의 에너지원으로는 충분하지 않다. 그 이유를 정량적으로 설명하라. (단 만유인력 상수 G≒7×10-11Nm2/kg2이다.)
3) 태양의 수소 중 핵융합 반응을 일으키는 요소는 중심부에 있는 약 15%다.
① 태양의 일생 동안 수소 핵융합 반응에 의해 발생하는 질량 결손을 구하라.
② 수소 핵융합 반응으로 생성되는 총 에너지의 양을 구하라. (단 광속도는 3×108m/s, 1년은 3.2×107초다.)
③ 수소 핵융합 반응으로 태양이 현재의 광도를 유지할 수 있는 기간은 얼마인가?
전문가 클리닉
1) 태양에서 발생하는 총 에너지가 보존되면서 구면으로 퍼져 나갈 때 지구에서 태양광선의 진행 방향에 대해 수직으로 놓인 단위면적에 도달하는 에너지양을 구합니다.
2) 태양에 존재하는 수소가 모두 연소될 때까지의 총 에너지양을 구하고 초당 발생 에너지양을 이용해 수명을 계산한 뒤 제시문과 비교합니다. 3) 간단한 수학적 계산으로 질량 결손과 핵융합 반응으로 생성되는 에너지양을 구하고 현재 광도를 고려해 태양의 잔여 수명을 계산합니다.