1. 비누로 만든 고체 연료
집에서 만들어보는 비누 연료
■ 준비물

비누, 칼, 금속제 컵 또는 열에 잘 견딜 수 있는 그릇, 냄비, 가스 렌지, 나무젓가락, 메탄올(약국에서 구입할 수 있음), 우유팩.
■ 실험방법

1. 세숫비누 10g(1/8정도 크기)을 준비해 칼로 곱게 갈아 가루로 만든다.

2. 냄비에 물을 조금 넣어 중탕 준비를 한다.
3. 금속제 컵에 메탄올 150mL와 비누를 넣고 중탕을 하면서 비누를 녹인다. 너무 뜨겁게 가열하면 메탄올이 다 날아가므로 주의한다.

4. 비누가 다 녹아서 용액이 되면 우유팩에 부어 식힌다. 굳기까지 여러 날이 소요될 수도 있다. 굳는 동안에는 저어본다거나 찔러보지 않도록 한다.
5. 굳어진 연료의 일부분이나 통째를 알루미늄 포일이나 깡통에 놓고 불을 붙여본다.

학교에서 만들어보는 고체 연료
■ 준비물

아세트산 칼슘, 메탄올(연료용 알코올), 빈깡통, 라이터나 성냥, 삼각 플라스크, 메스실린더(200mL, 100mL), 저울, 약수저
■ 실험방법

1. 아세트산칼슘 포화 용액을 만든다. 보통 물 100mL에 아세트산칼슘 40g을 녹인다.

2. 95%메탄올 150mL를 잰다.
3. 아세트산칼슘 포화수용액 30mL와 메탄올을 빈 깡통에 동시에 붓는다.

4. 젓지 말고 10초쯤 기다린 후 깡통을 뒤집어본다.

5. 뒤집어서 흘러내리지 않을 정도로 굳은 것이 확인되면 연료에 불을 붙여본다. 처음엔 불꽃이 잘 보이지 않으므로 주의한다.

■ 왜 그럴까?
비누 분자는 올챙이처럼 생겼는데, 그 사이의 틈에 메탄올 분자가 끼어 들어가면서 콜로이드 용액이 만들어진다. 그래서 비누가 녹는 것처럼 보이는데, 이 상태를 졸(sol)이라고 부른다. 이런 용액은 상태가 불안정해 열이나 약품에 의해 굳어져서 고체 또는 반고체 상태가 된다. 이것을 겔(gel)이라고 한다. 고체 연료는 메탄올과 비누의 겔 상태인 것이다.
아세트산칼슘 포화 용액에 메탄올을 섞으면 메탄올이 물과 섞이면서, 아세트산칼슘의 용해도가 줄어든다. 따라서 아세트산칼슘은 용액 전체에서 매우 빠르게 고체로 석출되면서 그물모양의 구조를 현성하게 된다. 이 그물은 메탄올을 잡아 가두면서 굳어지게 된다. 여기에 불을 붙이면 그물 사이에 갇혀있던 메탄올이 빠져 나오면서 타는 것이다.
신과람 박사의 실험파일
1. 아세트산칼슘 포화 용액을 만들 때는 물을 먼저 넣고 아세트산칼슘을 서서히 녹인다. 그래도 용액이 잘 만들어지지 않으면 며칠 동안 놔두면서 가끔식 휘저어준다. 용약의 윗부분이 투명해지면 그 용액을 따라서 사용한다.
2. 아세트산칼슘 자체는 희고 고운 분말인데, 어떤 경우에는 완전히 투명한 용액이 얻어지기도 하고, 연한 노란색의 용액이 얻어지기도 한다. 약품 제조 회사에 따라 순도가 다르기 때문에 녹는 모양이나 색깔 등이 상당히 다르다.
3. 아세트산칼슘용액과 메탄올은 동시에 섞어야 한다. 그렇지 않으면 어느 한쪽의 용액이 남게 된다.
4. 아세트산칼슘으로 만든 고체연료는 뚜껑을 덮어주는 것이 좋다. 그대로 놔두면 메탄올이 날아가면서 끈적거리는 용액 상태로 되돌아간다. 따라서 뚜껑을 덮을 수 있는 캔을 사용해 덮어서 보관한다. 실험이 끝난 후 남은 연료는 태워버리거나, 메탄올이 날아가게 놓아두었다가 남은 아세트산칼슘을 물에 녹여서 하수구에 버린다.
5. 비누로 만든 연료는 공기 중에 놓아두면 메탄올이 날아가면서 비누로 되돌아간다.
6. 고체 연료를 태울 때 입구가 좁고 긴 깡통에 고체 연료를 담으면 타다가 중간에 꺼지므로 입구가 넓은 깡통을 사용한다.
2. 얼룩무늬 티셔츠
크로마토그래피를 이용해 멋진 티셔츠를 만들어 나만의 여름을 연출해보자.
■ 준비물

흰색 티셔츠, 여러 가지 색깔의 유성매직, 에탄올(소독용 알코올), 신문지, 플라스틱 병.
■ 실험방법

1. 흰색 티셔츠 안쪽에 신문지를 여러 장 댄다.
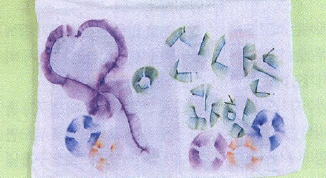
2. 티셔츠 위에 매직으로 원하는 글씨나 그림을 그린다.
3. 그림 위에 에탄올을 원하는 모양이 될 때까지 여러 방울 떨어뜨린다.
4. 환기가 잘 되는 곳에서 말린다.
■ 왜 그럴까?
크로마토그래피는 1903년 러시아의 베트라는 식물학자가 식물에 포함된 색소 성분을 분리하는 데 처음 사용했다. 물질의 종류에 따라 용매에서 이동하는 속도가 달라진다. 결국 움직이는 거리에 차이가 생기게 돼 혼합물을 이루는 적은 양의 성분 물질들도 분리하거나 확인할 수 있다. 이러한 원리로 잉크가 에탄올과 함께 이동하면서 멋진 무늬를 만들어낸다.
신과람 박사의 실험파일
1. 신문지를 두툼하게 대지 않으면 옷의 다른 면에 매직 잉크가 번진다.
2. 티셔츠 위에 그릴 모양은 폐곡선이나 문자가 좋다. 폐곡선 안이나 문자의 가운데에 에탄올을 떨어뜨리면 둥글게 퍼져나가면서 멋진 모양을 연출할 수 있다. 에탄올을 떨어뜨리는 위치와 양을 다양하게 조절하면서 자기만의 창작품을 만들어보자.
3. 밀폐된 공간보다는 환기가 잘되는 장소에서 작업을 한다.
미리 보는 가능 단풍색
■ 준비물

은행잎, 냄비, 우유팩, 원두커피 여과지, 에탄올, 온도계, 종이컵.
■ 실험방법

1. 같은 종류의 나뭇잎을 여러 장 모아서 잘게 자르거나 찢어 우유팩에 넣는다.

2. 우유팩에 에탄올을 나뭇잎이 충분히 잠길 정도로 넣는다.
3. 물 중탕을 하면서 에탄올 용액의 색깔이 변하는 것을 지켜본다. 에탄올의 온도가 지나치게 높이 올라가는 것(에탄올의 끓는점, 78.5℃)을 주의한다. 색깔이 변하면 우유팩을 냄비에서 꺼내 액체만 종이컵에 담는다.

4. 종이컵에 담긴 액체에 여과지가 약간 닿을 정도로 고정시킨다.
5. 일정 시간이 지나 색깔이 나타나면 종이를 말려서 색깔의 띠를 살펴본다.
■ 왜 그럴까?
식물들은 여름동안 자신이 필요로 하는 양분을 만들어낸다. 그들은 물과 공기중의 이산화탄소를 섭취하고, 태양빛을 이용해 녹말을 만든다. 이러한 과정을 광합성이라고 하는데 여기에는 잎이 녹색으로 보이게 하는 엽록소라고 하는 물질이 중요한 역할을 한다. 그리고 잎에는 엽록소 이외에도, 노랗게 보이게 하는 카로틴계의 색소와 붉게 보이게 하는 안토시아닌이라는 색소도 있다.
여름이 지나면 낮의 길이가 점점 짧아지고, 건조해진다. 이처럼 양분을 만들기에 좋지 않은 조건이 되면 식물들은 녹말 만들기를 중단하고, 녹색을 나타내는 엽록소는 사라지게 돼 그 동안 잎 속에 감춰졌던 다른 색의 색소가 나타나 단풍이 들게 된다. 크로마토그래피를 이용한 색소 분리 실험에서 녹색 이외에 노란색이 여과지에 나타났다면 올 가을에 이 잎은 노란색으로 물들 것이다.
한편 붉은색 단품의 경우는 메커니즘이 조금 다르다. 가을철이 되면 엽록소는 파괴되지만 잎 속의 당분은 증가한다. 이 당분의 증가가 붉은색을 나타내는 안토시아닌의 생성을 촉진하게 돼 잎이 붉게 변하는 것이다. 따라서 봄의 잎에 색소를 분리해 보면 붉은색의 색소는 거의 나타나지 않는다.
신과림 박사의 실험파일
1. 적어도 20분 이상 중탕 가열한다. 에탄올의 색깔이 진한 녹색으로 변할수록 결과가 잘 나타난다.
2. 가열할 때에 우유팩 안을 가까이 들여다보지 않는다. 기화된 에탄올이 눈 속으로 들어갈 수도 있다.
3. 색소를 분리할 때 에탄올은 유기용매로서 식물 세포막의 지질층을 녹여서 세포 속의 색소가 잘 빠져나올 수 있도록 도와준다.
4. 거름종이 대신에 도화지를 사용해도 가능하다.
3. 내가 만든 잠수함
여름에 해수욕장이나 풀장에 가서 잠수 솜씨를 뽐낼 수 있는 잠수함을 만들어 보면 어떨까? 바다나 풀장으로 가지고 갈 완벽한 잠수함을 만들기 위해 미니잠수함을 만들어보고 그 원리를 이용해 슈퍼잠수함도 만들어 보자.
■ 준비물

필름통, 페트병, 가는 빨대 2개, 굵은 빨대 2개, 작은 조약돌 20개, 고무찰흙, 송곳, 본도, 긴 컵
미니잠수함 & 슈퍼잠수함
■ 미니잠수함 실험방법
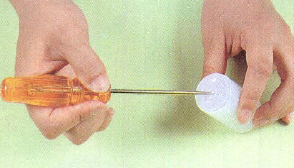
1. 송곳을 이용해 필름통 바닥에 5개 정도의 구멍을 골고루 뚫는다. 필름통의 2분의 1을 조약돌로 채운다.
2. 필름통 뚜껑에 구멍을 뚫어 빨대를 꽂고 빨대 주변의 빈틈을 본드와 고무찰흙을 이용해 잘 막는다. 이때 빨대는 2개를 연결해 길게 만든다.
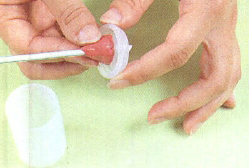
3. 뚜껑에 2개 정도의 구멍을 더 뚫는다.

4. 완성된 미니잠수함을 긴 컵에 넣고 스스로 가라앉으면 물 밖으로 나와 있는 빨대를 통해 공기를 불어넣어 다시 떠오르게 한다.
■ 슈퍼잠수함 실험방법
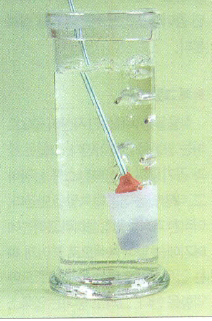
1. 페트병 뚜껑에서부터 5cm정도의 아래에 2개의 구멍을 마주보게 뚫고 빨대를 꽂는다. 이때 빨대는 각각 하나씩 쓰면 되고, 밖에서 안으로 기울어져 내려가게 꽂는다. 빨대의 반이 페트병 안쪽에 들어가 있으면 된다.

2. 빨대주변을 본드와 고무찰흙으로 잘 막는다.
3. 페트병 바닥에 골고루 여러 개의 구멍을 뚫고 조약돌을 2cm정도 쌓이게 넣어준다.

4. 페트병 뚜껑 바로 아래에 구멍 두 개를 내고 뚜껑을 꼭 잠근다.

5. 해수욕장이나 풀장에서 슈퍼 잠수함이 바닥에 생기면 같이 잠수해 공기를 불어넣어 준다. 페트병이 떠오르는 것을 볼 수 있다.
■ 왜 그럴까?
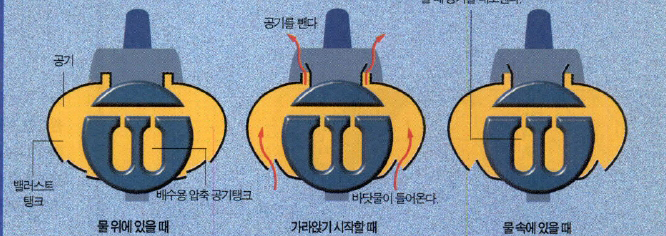
이 실험은 잠수함의 기본 원리를 단순화한 것이다. 잠수함의 부력을 조절하는 것은 잠수함 선체 양쪽에 있는 탱크이다. 이것을 밸러스트 탱크(bellast tank)라고 하는데 잠수함이 물위에 떠 있을 때는 공기로 가득 차 있게 된다. 잠수함이 물 속으로 들어갈 때는 탱크 안으로 바닷물이 들어오면서 선체가 무거워져 가라앉게 되는데, 어느 정도 깊이에서 떠있게 하려면 바닷물이 들어오는 밸브를 잠그면 된다.
가라앉았던 잠수함이 다시 떠오를 때는 선체 내부에 저장해 두었던 압축공기가 밸러스트 탱크 안에 밀려들어오면서 물을 잠수함 밖으로 밀어내어 가벼워져 뜬다. 이런 잠수함의 운동 역시 물에 대한 상대적인 밀도에 좌우되며 잠수함의 밀도가 물보다 작으면 뜨고, 크면 가라앉는다. 이 밀도는 밸러스트 탱크 안에 바닷물의 드나듦에 따라 조절된다(그림).
신과람 박사의 실험파일
1. 미니잠수함에는 가는 빨대를 사용하고, 슈퍼잠수함에는 굵은 빨대를 사용한다.
2. 슈퍼잠수함은 해수욕장이나 풀장에서 깊이 잠수해 공기를 불어주는 것이므로 빨대를 한 개만 사용해 만들어 준다.
3. 빨대를 꽂는 부분은 본드로 한번 붙이고 나서, 고무찰흙으로 감싸면 공기가 새지 않는다.
4. 빨대로 공기를 넣을 때 물을 빨아들이거나 삼키지 않도록 주의한다.