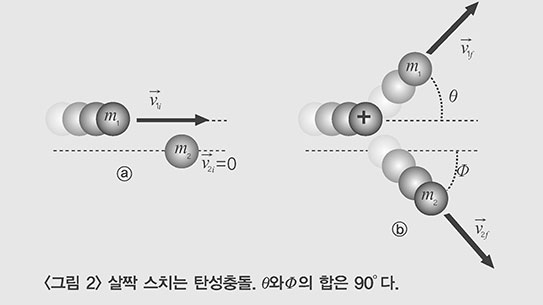
도체와 절연체(부도체)
철이나 구리, 알루미늄과 같은 금속은 전류가 잘 흐른다. 하지만 유리, 고무, 플라스틱과 같은 물질은 전류가 잘 흐르지 않는다. 전류가 잘 흐르는 물질과 그렇지 않은 물질에는 어떤 차이가 있을까? 물질은 원자로 구성된다. 원자는 중심에 양전하를 띠는 원자핵과 음전하를 띠고 원자핵 주위를 도는 전자들로 이뤄져 있다. 이 중, 원자핵으로부터 멀어서 쉽게 벗어날 수 있는 전자가 자유로운 상태에서 일정한 방향으로 흐르는 것이 전류다. 이와 같은 자유전자가 많아 전류가 잘 흐르는 물질을 도체라고 하고, 자유전자가 거의 없어서 전류가 잘 흐르지 않는 물질을 절연체(부도체)라고 한다. 도체에는 철이나 구리, 은, 알루미늄, 니크롬 등이 있고 절연체(부도체)에는 유리, 고무, 플라스틱 등이 있다.
전구가 연결된 전기회로 중간에 은, 구리, 니크롬과 같은 도체를 연결하면 전구에 불이 켜지는데 도체 종류에 따라 전구의 밝기는 다르다. 전류의 흐름을 방해하는 저항(값)이 도체마다 다르기 때문이다. 저항의 실체는 도체 속에서 진동하는 원자들이다. 이것이 자유전자들의 이동을 방해한다. 전자의 이동을 방해하는 정도를 수치화한 것을 ‘비저항’이라고 하며 물질의 종류에 따라 값이 다르다.
비저항은 단위면적당, 단위길이당 저항을 말하며 물질에 따라 값이 다르다. 비저항의 단위는 Ωm다. 물질이 전류를 얼마나 잘 흐르게 하는가를 나타내는 값인 전기전도도와 비저항은 서로 역수관계다.

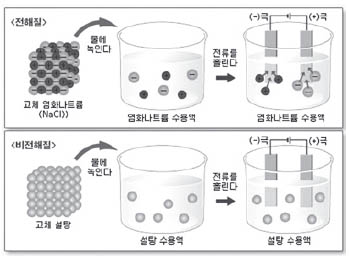
전류가 흐르는 액체, 전해질 용액
전류는 도체에서만 잘 흐르는 것이 아니다. 소금물 같은 액체에서도 전류가 잘 흐르는데, 이는 소금이 전해질이기 때문이다. 전해질은 물에 녹은 상태에서 이온으로 쪼개져 전류가 흐르는 물질이다. 대표적인 전해질로는 염화나트륨, 황산, 염산, 수산화나트륨, 수산화칼륨 등이 있다. 특히, 염화나트륨은 고체 상태에서는 전류를 흘려보내지 않아 절연체(부도체)지만, 수용액 상태에서는 전류를 흘려보내는 전해질이다.
물에 잘 녹는다고 모두 전해질은 아니다. 설탕도 물에 17잘 녹지만 설탕이 녹은 물에서는 전류가 흐르지 않는다. 소금의 주성분인 염화나트륨은 물에 녹으면 양전하를 띠는 나트륨 이온(Na+)과 음전하를 띠는 염화 이온(Cl-)으로 나뉜다. 하지만 설탕은 소금과는 달리 이온화되지 않는다. 설탕은 물에 녹아도 중성인 분자 상태로 존재하기 때문에 전류를 흐르게 하지 못하는 비전해질이다. 이처럼 소금과 설탕은 물에 녹을 때 약간 다르다.
전해질 용액에 전극을 연결하고 전압을 가하면 전기력에 의해 양이온은 (-)극 쪽으로 이동하고, 음이온은 (+)극 쪽으로 이동한다. 이것이 바로 용액을 통해 흐르는 전류다. 염화나트륨 수용액에서는 나트륨 이온이 (-)극 쪽으로, 염화 이온이 (+)극 쪽으로 이동한다. 전류의 방향은 나트륨 이온의 이동방향과 같다. 이처럼 전해질 용액에서 전류의 방향은 이온의 이동방향으로 결정된다. 일반적으로 전해질 용액의 경우, 물에 녹아 있는 이온의 농도가 높을수록 전류의 세기가 커진다. 하지만 일정 농도 이상이면 더 이상 전류의 세기가 증가하지 않는다.

컬러점토는 왜 전류가 잘 흐를까
도체와 전해질 용액에서는 전류가 잘 흐르고 절연체와 비전해질 용액에서는 전류가 잘 흐르지 않는다. 그런데 이런 도체와 액체의 전기적 특성을 모두 갖고 있는 물질이 바로 컬러점토다. 학교와 가정에서 교육용으로 다양하게 쓰는 컬러점토는 점토의 한 종류인데 전기적으로 도체에 가까운 성질을 갖고 있다. 물론 도선에 비해 저항은 크다.
컬러점토에는 어떻게 전류가 흐를 수 있을까? 비밀은 바로 컬러점토를 만드는 과정에 있다. 컬러점토를 만들 때 반죽에 쓰는 액체가 바로 소금물이다. 촉촉하고 말랑말랑한 컬러점토에는 전해질이 이온의 형태로 녹아 있어서 전압을 걸면 컬러점토를 통해 이온이 이동해 전류가 흐른다. 하지만 수분이 증발해 딱딱하게 굳은 컬러점토에서는 이온이 이동할 수 없어서 전압을 가해도 전류가 흐르지 않는다.
컬러점토처럼 촉촉하지만 전류가 흐르지 않는 것도 있다. 바로 고무찰흙이다. 고무찰흙은 전극을 걸어도 전류가 흐르지 않는 절연체다. 고무찰흙에는 염화나트륨과 같은 전해질이 녹아 있지 않기 때문이다. 고무찰흙은 컬러점토보다 약 100배 이상 큰 저항 값을 갖는다. 컬러점토와 고무찰흙, 이름이 비슷해서 성질도 비슷해 보이지만, 전기적 특성은 전혀 다르다. 이 둘을 이용하면 기본적인 전기회로는 물론 창의적인 과학·예술 융합 작품을 만들 수 있다.
컬러점토와 고무찰흙이 없이도 집에 있는 밀가루를 이용할 수도 있다. 밀가루를 반죽할 때 소금물을 섞으면 컬러점토처럼 전류가 흐르는 반죽이 된다. 밀가루에 설탕물을 섞으면 고무찰흙처럼 전류가 흐르지 않는 반죽이 된다. 컬러점토와 고무찰흙, LED 그리고 전지를 이용해 간단한 전기회로를 만들어 보자.
점토로 전지를 만든다
컬러점토는 지금까지 살펴본 것처럼 전류가 잘 흐를 수 있는 전도성 물질이므로 금속의 반응성 차이를 이용하면 과일전지와 같은 ‘전지’를 만들 수 있다. 금속의 반응성은 금속의 이온화 경향, 다시 말해 금속원자가 산화돼 양이온이 되려는 경향이다.

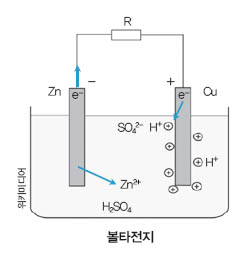
금속의 반응성 차이를 이용한 세계 최초의 전지는 이탈리아의 물리학자 볼타가 발명한 볼타전지다. 아연판과 구리판을 두 극으로 사용한 가장 간단한 전지다. 구리판과 아연판을 묽은 황산 용액에 담그고 구리판과 아연판을 도선으로 연결하면 전류가 흐를 수 있다. 구리에 비해 반응성이 큰 아연은 전자를 잃고 양이온 형태로 용액 속에 녹아 들어간다. 아연이 내놓은 전자는 전위차에 의해 도선을 따라 구리판으로 이동한다. 구리판에서는 용액 속 수소이온이 전자를 얻어 수소 기체로 환원된다. 이때 도선을 따라 이동하는 전자가 전류가 된다.
반응성이 서로 다른 두금속과 컬러점토를 이용하면 ‘점토전지’를 만들 수 있다. 이때 두 종류의 금속 여러 개와 비전도성 고무찰흙을 함께 사용하면 전지의 전압을 높이고 전지의 형태를 고정할 수 있다.
반응성 차이가 큰 금속의 조합일수록 더 많은 전자를 내어놓기 때문에 더 높은 전압이 형성된다. 일반적으로 LED를 켜기 위해 필요한 3V정도의 전압을 얻으려면 반응성 차이가 충분히 큰 두 금속을 사용한다.