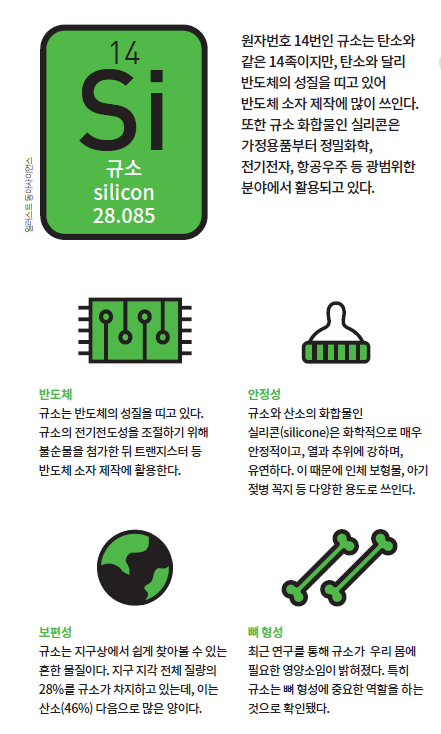
주기율표에서 탄소 바로 아래 위치한 규소. 때문에 규소를 탄소의 아류 원소 정도로 생각하는 독자가 있을지도 모르겠다. 하지만 규소는 탄소가 갖지 못한 중요한 특성이 하나 있다. 바로 반도체의 성질을 나타낸다는 것이다. 덕분에 규소는 현대 전자공학을 발전시킨 핵심 원소가 됐다. 정보기술(IT) 문명의 발전을 가능하게 만든, 지금의 정보화 사회를 이끈 주인공이 규소인 셈이다.

규소는 매우 특별하지만 동시에 매우 흔한 물질이기도 하다. 실제로 규소는 지구 표면에서 산소(46%) 다음으로 많은 원소다. 주로 모래나 흙, 돌에 들어있고, 지구 지각 전체 질량의 28%를 차지한다. 우주로 범위를 넓히면 8번째로 많이 존재하는 원소다.
" 준금속으로서 금속과 비금속의 성질을 모두 가진 규소는 반도체의 성질을 띤다.
인류는 이를 이용해 다양한 전자 소자 개발에 활용했다"
네 이름이 뭐니? silicon vs. silicone
규소에 대해 알아보기 전에 먼저 짚고 넘어갈 점이 있다. 규소의 영문명인 ‘실리콘’에 관한 것이다. 실리콘을 표기할 때 ‘silicon’과 ‘silicone’이 혼용되는 경우가 많다. 알파벳 e 하나 차이지만, 이 둘은 학술적으로 엄연히 다른 용어다.
주기율표의 14번째 원소인 규소를 지칭할 때는 ‘silicon’이 올바른 표기다. 반면 여기에 e가 붙은 ‘silicone’은 규소와 산소를 주성분으로 하는 고분자물질을 통틀어 부르는 단어다.
예를 들어 반도체 집적회로의 제조 공정에 필요한 실리콘 웨이퍼는 규소 단결정으로 제작하기 때문에 ‘silicon wafer’라고 쓰는 게 맞다. 하지만 대학 등 화학 연구실에서 자주 쓰이는 실리콘 오일은 규소와 산소가 교대로 연결된 규소 수지여서 ‘silicone oil’이라고 표기해야 한다.
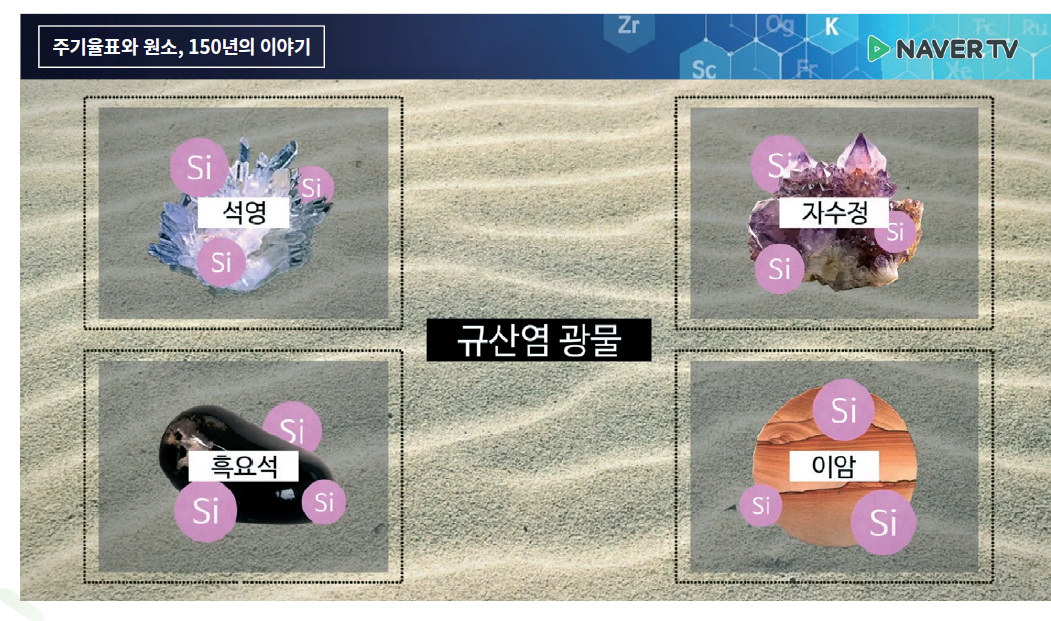
가장 간단한 규소 화합물 중 하나인 이산화규소(SiO₂)는 석영 또는 수정이라는 이름으로 잘 알려져 있다. 과거 부싯돌을 사용해 불을 붙이던 시대에는 주로 석영을 포함한 단단한 돌을 부싯돌로 활용했는데, 부싯돌을 나타내는 라틴어(silicis)가 바로 규소의 영어 이름의 어원이다.
그런데 산소와 규소가 워낙 단단하게 결합하고 있다 보니 그간 이산화규소에서 순수한 규소를 분리하기가 쉽지 않았다. 이를 처음으로 성공시킨 인물이 스웨덴의 화학자 옌스 야코브 베르셀리우스다. 베르셀리우스는 1823년 칼륨을 이용해 플루오린화규소(SiF4)에서 환원 반응을 일으켜 처음으로 규소를 홑원소 상태로 분리하는 데 성공했다.
당시 사람들은 새로 발견된 규소를 금속의 일종으로 생각했다. 따라서 금속 원소를 의미하는 어미(ium)를 붙여 ‘실리시움(silicium)’으로 불렀다. 하지만 나중에 규소가 금속이 아닌 것으로 밝혀지면서 1817년 스코틀랜드의 화학자 토머스 톰슨에 의해 비금속을 의미하는 어미(on)가 붙은 실리콘으로 바뀌었다. 지금도 유럽 일부 국가에서는 ‘silicium’으로 표기되기도 하지만, 국제순수·응용화학연합(IUPAC)에서 정한 올바른 표기는 ‘silicon’이다.
실리콘밸리, 실리콘비치… 첨단 반도체의 상징인 규소
규소는 탄소와 같은 14족 원소여서 이론적으로는 탄소처럼 4개의 공유결합이 가능하다. 하지만 규소는 원자가 탄소보다 1.5배 크고, 완전한 비금속인 탄소와 달리 준금속이어서 금속과 비금속의 성질을 모두 갖는다. 덕분에 규소는 탄소와는 다른 독특한 특성을 갖는다.
가장 큰 특성은 반도체라는 점이다. 규소는 도체처럼 전기를 통하게도 하고, 부도체처럼 전기를 통하지 않게도 한다. 일반적으로 전기전도성은 원자가띠*와 전도띠* 사이의 에너지 차이에 의해 결정된다. 반도체는 이 둘 사이의 에너지 차이가 매우 작아서 아주 적은 에너지만으로도 전자가 전도띠로 올라갈 수 있다. 전기전도성을 쉽게 제어할 수 있다는 뜻이다.
하지만 순수한 규소 결정은 전기전도도가 낮고 저항도 매우 크다. 이 때문에 규소에 불순물을 소량 첨가해 전기전도성을 조절하기 좋게 만든 뒤 반도체 소자 제작에 쓴다.
반도체는 불순물을 어떻게, 또 얼마나 첨가하느냐에 따라 특성을 손쉽게 바꿀 수 있다. 불순물의 종류는 크게 N형과 P형 두 가지로 나뉜다. N형 불순물은 규소보다 원자가전자가 하나 많은 인(P), 비소(As), 안티모니(Sb), 비스무트(Bi) 등이 쓰인다. N형 불순물이 포함된 규소는 공유결합을 하지 않는 여분의 전자를 갖게 된다. 여분의 전자는 쉽게 들떠 전도띠로 올라갈 수 있어 반도체 성질을 갖게 만든다.
반대로 붕소(B), 알루미늄(Al), 갈륨(Ga), 인듐(In) 등 P형 불순물은 규소보다 원자가전자가 하나 적어 공유결합에 필요한 전자가 부족하다. 이들 원소는 공유결합을 완성하기 위해 주변의 다른 원자 간 공유결합에서 전자를 하나 빼앗아오고, 이 과정이 반복되면서 전자가 이동한다.
더 재미있는 점은, 이런 P형 반도체와 N형 반도체를 접합하는 ‘P-N 접합’을 통해 한 방향으로만 전류가 흐르는 소자인 다이오드를 만들 수 있다는 것이다. 인류는 이를 이용해 트랜지스터 같은 전자 소자의 발전을 이룩해 왔다.
IT 기술에서 규소의 위상은 첨단과학기술단지의 이름에서도 엿볼 수 있다. 미국 캘리포니아주 샌프란시스코 남쪽의 첨단 IT 연구단지인 실리콘밸리는 반도체 등 첨단 소자에 들어가는 규소(실리콘)에서 이름을 따왔다. 또 로스앤젤레스 서부 산타모니카 해변에는 구글, 유튜브, 페이스북 등 많은 글로벌 IT 기업이 자리 잡고 있어 실리콘비치로도 불린다.
뼈 튼튼하려면? 칼슘보다 규소가 중요
반도체 이외에도 규소는 우리 주변의 다양한 곳에서 찾아볼 수 있다. 그중에서도 규소와 산소로 이뤄진 사슬에 탄소 등 다른 원소가 결합한 실리콘(silicone)은 내열성과 화학적 안정성이 뛰어나 여러 분야에 쓰이고 있다.
가령 규소와 산소가 연속적으로 결합한 폴리실록세인(polysiloxane)은 유연성과 압축률이 우수하고, 열과 추위 모두에 강하며, 쉽게 분해되지 않는다. 폴리실록세인의 이런 특성은 가정용품부터 정밀화학, 전기전자, 자동차, 항공우주산업에 이르기까지 광범위한 분야에서 활용되고 있다. 창틀을 메우는 실란트와 자동차 유압식 브레이크의 기름도 폴리실록세인으로 만든다.
실리콘은 인간의 피부 조직과 매우 흡사하면서도 체내에서 안정된 구조를 유지할 수 있어 체내 보형물 재료로도 사용된다. 고온에서 환경호르몬을 배출하지 않아 고온 살균이 필요한 아기 젖병의 꼭지도 실리콘으로 만든다.
규소는 생명체가 생명을 유지하는 데 없어서는 안 될 영양성분이기도 하다. 이런 사실이 알려진 건 그리 오래된 일은 아니다. 토양을 이루는 주성분인 규소는 곡물이나 과일, 채소 등을 섭취하면서 자연스럽게 체내에 흡수된다. 비록 체내에는 5g 미만인 미량으로 존재하지만, 규소는 피부와 장기, 골격 등 신체 전체에 분포한다. 특히 포유류의 경우 뼈, 연골, 힘줄, 혈액 등 결합조직에 가장 풍부하다.
그중에서도 규소는 특히 뼈 형성 과정에 많이 관여하는 것으로 알려져 있다. 1970년대 진행된 프레이밍햄 자손 연구가 대표적이다. 당시 미국 매사추세츠주 프레이밍햄이라는 도시에서는 주민 약 2800명을 대상으로 식생활과 건강 상태에 관한 조사가 진행됐다. 조사 결과 규소 섭취량이 요추와 대퇴골 경부의 골밀도에 밀접하게 관련돼 있다는 사실이 밝혀졌다.
특히 남성과 폐경 전 여성의 경우 규소 섭취량이 많을수록 대퇴골 경부의 골밀도가 높은 것으로 나타났다. 무엇보다도 이 연구에서 눈길을 끈 사실은 규소 섭취량과 골밀도 사이의 연관성이 칼슘 섭취량과 골밀도 사이의 연관성보다 더 크다는 점이었다. 뼈를 튼튼하게 만드는 무기염류로 잘 알려진 칼슘보다 규소가 뼈를 더 단단하게 한다는 뜻이다.
국제학술지 ‘BMC 근골격계 장애’ 2008년 6월 11일자에 발표된 논문에 따르면 규소는 비타민과 칼슘의 보조 성분으로 작용해 뼈 형성을 촉진한다. doi: 10.1186/1471-2474-9-85 연구팀은 임상시험을 통해 규소를 칼슘 및 비타민 D3과 함께 섭취할 경우 규소 없이 칼슘과 비타민 D3만 섭취할 때보다 뼛속 콜라겐이 더 많이 형성돼 골다공증 예방에 도움을 줄 수 있다는 사실을 확인했다.
이렇듯 규소라는 원소는 화학뿐만 아니라 전자공학, 재료공학, 생명과학에 이르기까지 다양한 분야에서 핵심 원소로 활약하고 있다. 또 앞으로는 인공지능(AI) 기술이 4차 산업혁명의 핵심으로 꼽히는 만큼 이를 처리하기 위한 IT 기술에 대한 수요가 더욱 증가할 것이고, 이에 따라 규소의 역할도 커질 것이다. 규소가 인류의 발전을 위해 빼놓을 수 없는, 세상을 ‘바꿀’ 원소라는 데 의문의 여지가 없다.
김희진
일본 오카야마대 응용화학과를 졸업한 뒤 교토대에서 유기합성화학으로 박사학위를 받았다. KAIST와 POSTECH(포항공대)에서 연구원을 지낸 뒤 일본 교토대에서 특임교수로 재직했다. 현재는 고려대 화학과 교수로 유기화학 분야를 연구 중이다.
heejinkim@korea.ac.kr

*용어정리
원자가띠(valence band)
절대영도(0K)에서 전자가 존재하는 가장 높은 전자 에너지 범위.
전도띠(conduction band)
전자가 비어있는 가장 낮은 에너지 범위. 부도체와 반도체의 경우 전도체와 원자가띠 사이에 에너지 차이가 있다.