가는 관을 심장에 넣어 혈액의 흐름을 조사하는 심장카테터법을 개발한 독일인 의사 베르너 포르스만은 심장질환 치료의 신기원을 열었다. 이 공로로 그는 1957년 노벨생리의학상을 받았다. 그런데 그가 심장카테터법을 개발하고 연구결과를 발표한 1930년대 세상의 반응은 냉담했다. 병원은 그를 해고했고 독일정부는 심장카테터법 연구를 25년간 금지할 정도였다. 이유는 그가 직접 자신의 심장에 전극을 심어 실험했기 때문. 비인간적인 연구방법 때문에 그는 노벨생리의학상을 받기 전까지 ‘서커스 곡예를 부리는 사기꾼’이라는 오명을 써야 했다.
아무리 멋진 연구성과라도 과학자가 자신의 목숨을 담보로 실험한다면 위험하다. 이 때문에 실험동물이 중요하다. 포르스만 박사가 상을 받은 지 50년이 지난 2007년. 노벨생리의학상 수상의 영광은 특정 질병을 앓는 ‘맞춤형 쥐’를 만들어 실험할 때 동물을 이용하는 토대를 마련한 미국 유타대 유전생물학과 마리오 카페키(70) 교수, 영국 카디프대 포유류유전학과 마틴 에번스(66) 교수, 미국 노스캐롤라이나대 병리학과 올리버 스미시스(82) 교수에게 돌아갔다.

사극에서 기미상궁 역할
맞춤형 쥐는 ‘유전자 적중 쥐’(Gene targeting mouse)라 불리는데, 사극에 나오는 ‘기미상궁’에 빗댈 수 있다. 기미상궁은 왕이 식사를 하기 전 음식에 독이 들었는지 미리 맛을 보던 신하다. 유전자 적중 쥐를 이용하면 질병 치료 방법이나 치료제를 미리 실험한 뒤 인체에 사용해도 안전한지 미리 검증할 수 있다. 유전자 적중 쥐를 만든 ‘트로이카’가 “우리는 긴급구조대보다 사람의 목숨을 더 많이 구했다”고 말한 것도 일리 있는 셈이다.
카페키 교수와 스미시스 교수는 포유류 배아줄기세포의 유전자를 변형해 유전자의 기능을 정확히 밝히고, 각종 질병을 치료할 수 있는 토대를 마련한 공로를 인정받았다. 이들은 1985년부터 1990년까지 연구결과를 앞 다퉈 발표하던 경쟁자이기도 했다. 그리고 에번스 교수는 포유류인 쥐의 배아줄기세포를 발견해 카페키와 스미시스 교수의 연구를 뒷받침했다.
트로이카가 쌓은 연구결과는 유전자 적중 쥐라는 결과물을 만들어냈다. 이들은 1987년 쥐의 배아줄기세포 염색체에서 약 3만개의 유전자 가운데 원하는 부위를 정확히 제거하는 ‘유전자 적중 기술’을 개발했다. 1989년에는 유전자 적중 쥐를 세상에 처음으로 선보였다. 원하는 유전자를 정확하게 제거할 수 있는 유전자 적중 쥐는 질병을 치료하는 길을 매끄럽게 닦았다.
맞춤형 쥐는 과학자가 원하는 특정 유전자를 쏙 뺀 쥐다. 사실 특정 유전자를 없애거나 다른 유전자로 바꾸는 기술은 미생물 같은 하등동물에서는 이미 개발됐다. 병충해에 강한 작물 같이 유전자를 변형하는 유전공학기술은 생소하지 않다. 그런데 동물의 유전자를 조작할 땐 더 많은 문제를 생각해야 한다. 1조개가 넘는 동물의 모든 세포에서 특정 유전자를 빼기란 쉽지 않기 때문이다.
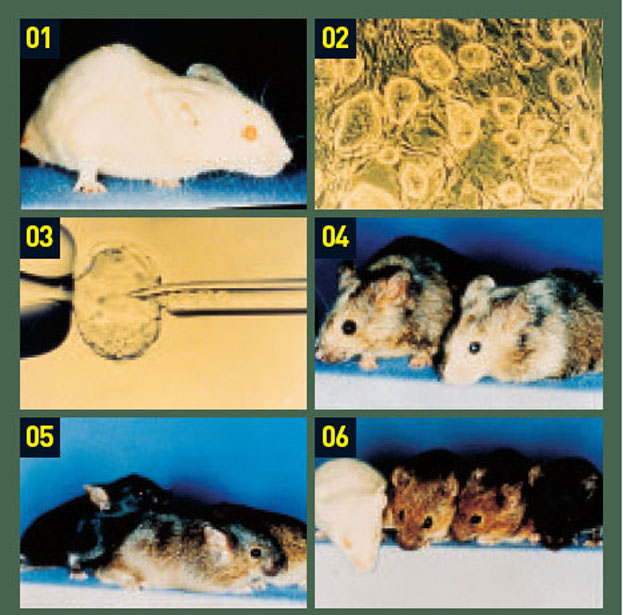
유전자 하나만 쏙 골라 뺀다
동물을 대상으로 특정 유전자를 빼려면 세포 수가 적을 때, 즉 발생 단계 초기인 배아 상태에서 유전자를 바꿔야 한다. 카페키 교수와 스미시스 교수는 배아줄기세포에서 없애고자 하는 유전자(예를 들어 A 유전자)를 잘라 사이에 네오마이신 저항유전자를 끼워넣고 연결해 ‘유전자 운반체’에 삽입했다. 이 운반체를 배아줄기세포에 전기충격으로 넣으면 세포 내 유전체에서 같은 부위를 찾아 유전자를 교환한다. 즉 유전자 운반체가 생물이 원래 가지고 있던 유전체에서 특정 유전자를 제거하는 셈이다.
유전자를 교환한 유전체만 골라내는 방법도 중요하다. 교환 성공률은 100만분의 1로 낮은 편이다. 운반체와 유전자를 교환한 세포는 A 유전자가 제거된 곳에 네오마이신 저항유전자가 들어가 항생제인 네오마이신을 포함한 세포배양 배지에서도 살아남는다. 반면 유전자가 재조합되지 않은 세포는 죽는다. 이렇게 연구자는 원하는 유전자를 가진 세포를 얻을 수 있다.
이렇게 얻은 세포를 털 색깔이 다른 쥐의 배반포 단계 수정란에 미세피펫으로 넣는다. 그리고 수정란을 대리모 쥐의 자궁에 이식한다. 그 결과 키메라 쥐(발생 단계에서 특정 유전자를 없앤 세포와 정상세포가 섞인 쥐)가 태어나는데 키메라 쥐를 줄기세포를 만든 같은 품종의 쥐와 교배해나가면 유전자를 100% 완벽하게 변형한 쥐를 만들 수 있다.
지금까지 태어난 유전자 적중 쥐는 약 1000종류다. 한 예로 1994년 미국 록펠러대 제프리 프라이드만 교수는 렙틴이라는 유전자를 없앤 유전자 적중 쥐를 생산했다.
렙틴은 포만감을 느끼게 하는 단백질인데, 렙틴이 없으면 항상 배고픔을 느낀다. 렙틴이 없는 쥐는 정상 쥐에 비해 체중이 2배 이상 무겁다. 그는 유전자가 비만을 일으킬 수도 있다는 사실을 발견해, 이제까지 비만은 게으르거나 식습관에 문제가 있을 때 생긴다는 고정관념을 깼다.
또 렙틴 유전자를 없앤 쥐는 연구소에 큰 이윤을 안겨주기도 했다. 프라이드만 교수는 이 쥐를 여러 회사에 고가로 팔았을 뿐 아니라 암젠이라는 회사에 2000만 달러(한화로 180억 가량)를 받고 특허권을 이양했다.
2001년 유방암 치료약인 허셉틴을 복용한 환자가 심장병 부작용으로 귀중한 생명을 잃은 사건이 있었다. 그런데 2002년 허셉틴을 유전자 적중 쥐에 실험한 결과 심장병을 일으키는 부작용이 발견됐다. 유전자 적중 쥐를 조금만 더 일찍 만들어 해당 약을 실험했다면 인명 피해가 없었을 지도 모른다. 과학자들이 유전자 적중 쥐에 관심을 기울이는 이유다.
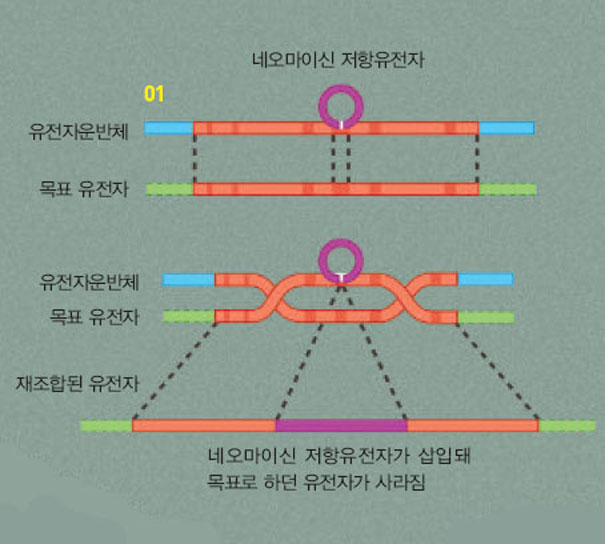
01 특정 유전자를 없앤 유전자 적중 쥐를 만들기 위해 없애고자 하는 유전자와 네오마이신 저항유전자를 유전자운반체에 삽입한 뒤 변화시키고자 하는 유전자 가닥과 교차를 일으킨다.
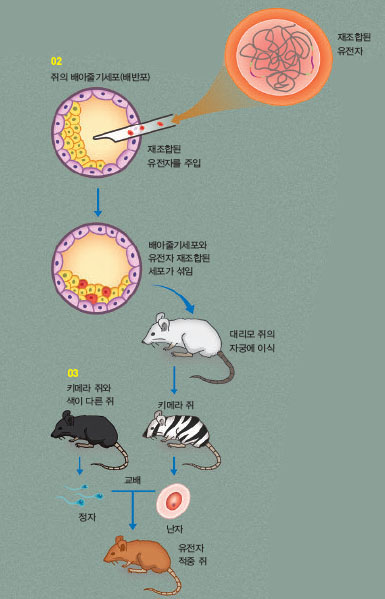
02 특정 유전자를 없앤 세포를 배반포 단계인 쥐의 배아줄기세포에 넣으면 유전자가 재조합된 세포가 배반포 단계의 세포와 섞인다.
03 배아줄기세포를 대리모 쥐의 자궁에 이식하면, 유전자를 변형시킨 세포와 정상세포가 섞인 키메라 쥐가 태어난다. 키메라 쥐를 그와 색이 다른 쥐와 교배해 나간다. 결국 특정 유전자를 갖지 않은 유전자 적중 쥐가 만들어진다.
파일럿 스미시스와 의지의 과학자 카페키

2007년 노벨생리의학상을 받은 트로이카 가운데 두 과학자는 불굴의 의지를 갖춘 과학자다.
스미시스 교수는 경비행기인 세스나 182기를 조종하는 파일럿이다. 1995년 미국의 유명 비행잡지에 경비행기를 12만km 이상 운항한 사람으로 소개됐을 정도다. 학회에 갈 때도 항상 자신의 비행기를 타고 이동한다. 이유는 한 가지. 시간을 절약하기 위해서다.
그는 연구를 최우선으로 두고 생활계획을 세운다. 이 때문에 벌어진 일화도 있다. 어느 날, 실험시간에 늦은 그는 실험을 망칠지도 모른다는 초조함에 과속운전을 했다. 속도위반으로 경찰에 붙잡힌 것은 당연한 일. 그런데 그는 운전면허증을 요구하는 경찰에게 파일럿 자격증을 보여줬다. 경찰은 웃으면서 그를 훈방했다. 이렇듯 자투리 시간도 아끼고 연구에 책임감을 느끼는 태도가 유전자 적중이라는 획기적인 기술 개발을 가능하게 한 것인지도 모른다.
카페키 교수도 이에 못지않다. 그가 세 살 이던 1941년 파시즘에 반대하는 어머니가 게슈타포에 체포돼 독일 정치수용소에 수용됐다. 어머니의 보살핌을 받지 못한 그는 어느 농부의 보살핌을 받았으나 곧 거리로 내몰렸다. 그 뒤 그는 홀로 거리를 방황하다 고아원에 들어갔다.
2차 대전이 끝나 감옥에서 풀려난 어머니는 병든 몸으로 아들을 극적으로 만났다. 미국에 물리학자로 있던 삼촌의 도움으로 그는 어머니와 미국으로 이민을 와서 공부를 할 수 있었다.
1980년대 그의 연구주제는 암이나 고혈압, 당뇨병, 알츠하이머와 같은 불치의 병을 고칠 수 있는 줄기세포 배양연구였다. 카페키 교수는 어린 시절 어머니와 헤어져 배고프고 병들었던 뼈아픈 기억을 마음에 담고 있다. 가난과 질병에 대한 그의 깊은 연민이 이러한 연구로 발전한 것이 아닐까.
▼관련기사를 계속 보시려면?
2007년 노벨과학상 따라잡기
1. 하드디스크 소형화 일등공신 거대자기저항
2. 암모니아 합성 과정, 원자 수준에서 보는 고체표면화학
3. 줄기세포로 사람 살리는 맞춤형 쥐
칼 삼키는 묘기, X선으로 파헤치다